
在疫苗、细胞与基因治疗(CGT)等先进生物制药的生产中,贴壁细胞的消化和传代是关键工艺步骤,高度依赖胰蛋白酶类试剂,其中Gibco TrypLE、上海逐典TrypLUS等重组胰酶类似物已成为行业主流,能有效保障细胞活性与工艺稳健性。随着全球监管机构对生物制品工艺相关残留杂质的要求日趋严格,建立可靠合规的胰蛋白酶残留检测方法,成为质量控制(QC)体系的核心环节,而“消化”与“检测”的同源匹配,是应对该挑战的理想解决方案。同源匹配核心是让生产用消化酶与残留检测试剂盒的抗原-抗体识别系统来自同一家供应商,可显著提升检测准确性、保障结果一致性,规避不同供应商产品批间差异的干扰。逐典生物推出的TrypLUS“消化+检测”完整产品组合,是国内少数可同时提供工艺用消化液与配套残留检测试剂盒的方案,全方位支持药企从工艺开发到质量放行。其中,TrypLUS消化液为非动物源性重组胰酶类似物,温和高效、稳定性强,已完成FDA的DMF备案且符合GMP标准;配套ELISA检测试剂盒与消化液同源匹配,特异性强、灵敏度高(检测下限低至0.625 ng/mL),性能参数完全符合药品放行要求。该方案通过同源匹配理念,实

在生物医学研究、细胞治疗和生物制药等前沿领域,实验样本及生产过程中残留的核酸(DNA/RNA)是常见干扰源,不仅会影响实验结果(如蛋白纯度、病毒滴度),还可能引发免疫反应、导致生物制品降解。全能核酸酶作为可高效降解所有形式核酸的酶制剂,能非特异性降解单链、双链、线状及环状核酸,堪称实验室和生产线上的“清洁大师”,核心价值在于提升样本及产品纯度、保护目标产物、优化下游生产工艺。根据样本盐离子浓度,全能核酸酶可分为普通型与耐高盐型,遵循“低盐选普通,高盐选耐盐”的选择原则,适配不同应用场景。其经典应用涵盖蛋白纯化、病毒载体(AAV、慢病毒)生产、细胞治疗产品制备,各场景均有明确的用量、处理参数及应用效果,可满足《中国药典》等相关法规对产品纯度的严格要求。使用过程中需注意温度控制、避免抑制剂干扰及下游酶去除等事项,确保酶活性与工艺合规。在技术前沿领域,逐典生物通过AI酶进化与重组蛋白定向改造平台,开发出高性能Pannarase系列全能核酸酶,该系列产品具备高酶活性、高产物回收率、高工艺简便性等优势,提供从标准型到高盐耐受型(SAN)的全系列产品,可精准适配病毒纯化、疫苗生产、蛋白/多糖制药等

在活体生物发光成像技术中,D-萤光素与萤光素酶的结合是实现生物体内“可视化”的核心化学基础。为帮助科研人员获得高信噪比、可重复的成像结果,本文系统性解析D-萤光素的选择方法及规范操作流程。活体生物发光成像本质是酶促化学反应,核心参与者包括北美萤火虫来源的萤光素酶(Fluc)、生物活性底物D-萤光素及ATP、氧气、镁离子等辅因子,萤光素酶催化D-萤光素氧化释放可见光,而D-萤光素作为手性分子,仅D型构象可被酶识别,因此高纯度是实验成功的首要条件。选择D-萤光素时,需权衡钠盐与钾盐:钠盐水溶性好、稳定性强、应用广泛,适配常规肿瘤模型成像等场景;钾盐饱和溶解度更高、溶解更快,适合高浓度、小体积给药的特殊实验。市售D-萤光素纯度差异影响成像信噪比与性能,常规实验选择≥98%纯度即可,挑战性场景需优先选用高纯度产品。此外,需根据体内、体外不同实验场景调整使用策略,体内成像注重底物的达峰时间、平台期稳定性及药代动力学一致性,体外检测则侧重高瞬时亮度与快速反应速度。同时,规范储存、配制、剂量控制等操作细节,也是保障成像效果的关键,助力科研人员高效开展活体生物发光成像相关研究。
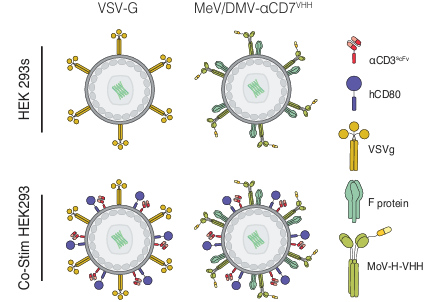
CAR-T疗法虽在复发难治性血液肿瘤中展现出治愈潜力,但传统自体CAR-T体外制备流程漫长、成本高昂、可及性低,“体内生成CAR-T”被视为下一代细胞疗法的核心方向,却面临递送效率、T细胞靶向特异性、人体预存免疫清除三大核心挑战。2026年4月6日,《自然·通讯》在线发表了Broad Institute和麻省总医院团队的重磅研究,通过新型慢病毒载体设计,在三大难题上实现显著突破。该研究构建了“DMV假型包膜+纳米抗体靶向域+CD7靶点”的三重协同设计:以海豚麻疹病毒(DMV)为包膜实现免疫逃逸,规避人体预存中和抗体;采用骆驼源纳米抗体(VHH)提升靶向效率,解决传统scFv的固有缺陷;选择CD7作为靶点,实现T细胞的精准识别与转导。实验数据显示,该新型慢病毒载体在体外转导效率高、特异性强,在人源化小鼠模型中可高效生成功能性CAR-T细胞,显著降低肿瘤负荷、延长生存期,且安全性良好。本文深度剖析该研究的技术细节、创新价值及行业影响,对比现有体内递送技术路径,分析其临床转化面临的生产工艺、长期安全性等挑战,并指出该技术对CAR-T商业格局的变革意义,以及中国生物医药产业在纳米抗体、CDMO

肿瘤免疫治疗作为继手术、放疗、化疗之后的第四大肿瘤治疗模式,核心是通过激活或重塑机体自身免疫系统,打破肿瘤免疫逃逸,实现对肿瘤细胞的精准识别与杀伤,相较于传统治疗具有特异性强、疗效持久、副作用温和等优势,已在多种恶性肿瘤中取得突破性进展。本文基于临床与科研共识,对肿瘤免疫治疗进行层级化分类,构建了完整的体系框架,主要分为五大核心类别。其中,免疫检查点抑制剂是最成熟、临床应用最广泛的类别,涵盖PD-1/PD-L1、CTLA-4抑制剂等,覆盖数十种实体瘤及血液肿瘤;过继性细胞免疫治疗属于精准个体化治疗,以CAR-T、TCR-T、TIL等细胞疗法为核心,在血液肿瘤中疗效显著,同时逐步向实体瘤突破;肿瘤疫苗分为预防性与治疗性两类,可激发机体长效免疫,用于肿瘤预防与辅助治疗;单克隆抗体药物兼具靶向与免疫功能,包括靶向抗体及ADC药物,实现精准靶向杀伤;非特异性免疫调节剂则通过广谱激活免疫系统,作为联合治疗的辅助手段。此外,本文还梳理了各类疗法的联合策略,分析了当前面临的挑战,并展望了精准化、普惠化的未来发展方向,为全面理解肿瘤免疫治疗的分类、机制与临床应用提供清晰指引。
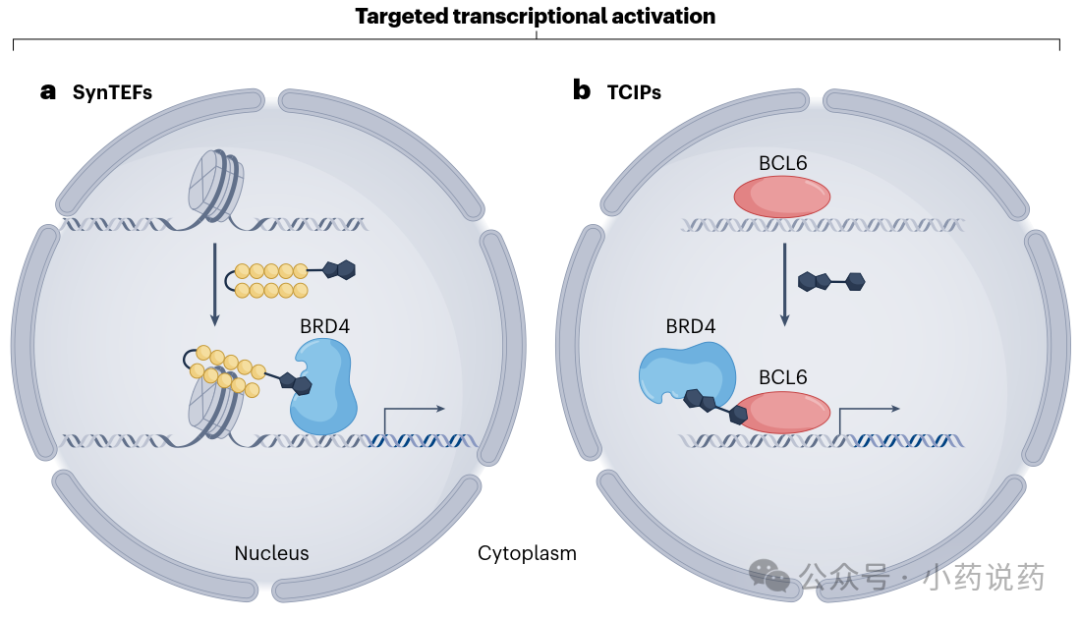
传统小分子药物发现依赖占据驱动药理学,但其无法触及约80%缺乏化学配体的“不可成药”蛋白靶点,在此背景下,“事件”驱动药理学应运而生,核心是通过诱导邻近(小分子或生物制剂诱导两个大分子复合化),绕过对功能性抑制剂或活性位点结合剂的需求,成为破解不可成药靶点的关键策略。诱导邻近模式主要分为分子胶和双功能分子两大类,二者虽曾被视为不同,但其区别更多在于蛋白界面相互作用及三元复合物的协同性,形成连续谱系。本文系统梳理诱导邻近模式疗法的核心内容:分子胶从天然产物(环孢素A、雷帕霉素)到合成制剂(沙利度胺类似物、RMC-6236),实现从偶然发现到理性设计的跨越,可通过降解、抑制或稳定机制发挥作用;双功能诱导邻近药物涵盖化学诱导二聚化(CID)、蛋白降解靶向嵌合体(PROTACs),其中PROTACs已成为极具前景的治疗模式,已有药物获批上市且可克服耐药性;同时拓展了超越细胞内靶点的靶向蛋白降解技术,依托自噬体-溶酶体、内体-溶酶体途径,实现错折叠蛋白、细胞表面及胞外蛋白的降解;此外,还包括翻译后修饰双功能调节剂、蛋白功能双功能调节剂等前沿方向。诱导邻近模式疗法已取得显著临床成功,未来通过结构导