文章来源公众号:生物快评 作者:sw
David Baker,2024诺贝尔化学奖的主,华盛顿大学教授
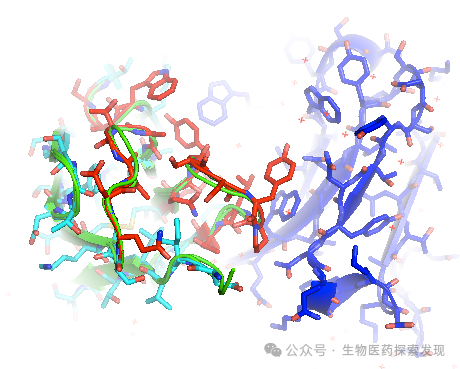
2025年9月29日David Baker,2024诺贝尔化学奖得主发表了一篇《Computational design of pH-sensitive binders》,这篇文章利用对Binder的结合界面增加组氨酸来让其具有pH的敏感性。
背后生化化学原理
氨基酸的结构上,一端为氨基NH2,一端为COOH基团,中间为一个CH,其中CH上为侧链基团,R基团的差异就会导致氨基酸性质的改变。那么根据R基团的差异,可以将氨基酸分成4类:非极性氨基酸(就是不电离,不亲水的氨基酸);极性氨基酸(就是不带电,但是亲水的氨基酸);碱性氨基酸(即在中性pH下带正电的氨基酸);酸性氨基酸(即在中性pH下带负电的氨基酸)。
20种氨基酸分类表(4大类)
氨基酸的电解和电离常数pKa
因为氨基酸同时具有酸性基团COOH和碱性基团NH2,且有些R基团会额外电离,所以每个氨基酸的每个基团都有自己的电离常数,pKa。pKa 是衡量一个酸强弱的定量指标。
Ka 是这个解离反应的平衡常数,其表达式为:
其中,[ ] 表示浓度。pKa值越小,酸性越强;pKa值越大,酸性越弱。
pKa 是Ka 的负常用对数:
氨基酸的电解,比如每个氨基酸都有电解常数1pKa1(COOH电解释放H+的能力),NH2基团的电解常数pKa2(即NH2释放H+的能力)。其中有7个氨基酸的R基团也能够电离,所以他们额外有了pKR(即R基团电离释放H+的能力)。
这7个氨基酸即3个碱性氨基酸LysineArgineHistidine,2个酸性氨基酸aspartic acid和glutamic acid。
以及1个亲水性的Cysteine,因为其侧链含有巯基(R-SH),该基团在碱性环境中可作为质子供体,失去质子后形成硫醇阴离子(R-S⁻);一个疏水性的Tyrosine(酪氨酸的酚羟基可发生去质子化,该化学特性与苯酚(由苯环和氧原子构成)类似,固有pKr)。
氨基酸的等电点
如刚才介绍的氨基酸的电离常数,可以发现氨基端和羧基端和部分的R基团都对氨基酸的整体电离有贡献作用,此外氨基酸所处在的环境pH也会影响氨基酸的电离。溶液环境的pH值决定了这些基团的解离状态:
在低pH(酸性)环境中,溶液中的H⁺浓度高,会抑制羧基的解离,并促使氨基结合H⁺。因此,氨基酸整体带正电荷。
在高pH(碱性)环境中,溶液中的OH⁻会中和H⁺,促使羧基解离释放H⁺,同时氨基也难以结合H⁺。因此,氨基酸整体带负电荷。
随着pH值从低到高变化,氨基酸的净电荷会从正电荷逐渐变为负电荷。在这个变化过程中,必然存在一个特定的pH值,使得氨基酸的正负电荷数恰好相等,净电荷为零。这个pH值就是该氨基酸的等电点(pI)。
如下图给出了20个氨基酸的pKa和pI值。
Amino Acid | Abbreviation | Structure | MW | pKa (25 °C) | pI (25° C) | |||
-CO2H | -NH2 | Side chain R | ||||||
Alanine | Ala | A | | 89.10 | 2.35 | 9.87 | 6.11 | |
Arginine | Arg | R | | 174.20 | 1.82 | 8.99 | 12.48 | 10.76 |
Asparagine | Asn | N | | 132.12 | 2.14 | 8.72 | 5.43 | |
Aspartic Acid | Asp | D | | 133.11 | 1.99 | 9.90 | 3.90 | 2.98 |
Cysteine | Cys | C | | 121.16 | 1.92 | 10.70 | 8.37 | 5.15 |
Glutamic Acid | Glu | E | | 147.13 | 2.10 | 9.47 | 4.07 | 3.08 |
Glutamine | Gln | Q | | 146.15 | 2.17 | 9.13 | 5.65 | |
Glycine | Gly | G | | 75.07 | 2.35 | 9.78 | 6.06 | |
Histidine | His | H | | 155.16 | 1.80 | 9.33 | 6.04 | 7.64 |
Isoleucine | Ile | I | | 131.18 | 2.32 | 9.76 | 6.04 | |
Leucine | Leu | L | | 131.18 | 2.33 | 9.74 | 6.04 | |
Lysine | Lys | K | | 146.19 | 2.16 | 9.06 | 10.54 | 9.47 |
Methionine | Met | M | ||||||