本文来源于微信公众: 药化文献搬运 作者: 博一的小马

一、ADC在肿瘤治疗中的研究背景
抗体偶联药物(Antibody-Drug Conjugates,ADCs)是一类将细胞毒性小分子药物通过化学连接体共价连接至单克隆抗体上的靶向治疗药物。该策略旨在利用抗体对肿瘤抗原的特异识别能力,实现高效细胞毒载荷在肿瘤部位的定向递送。
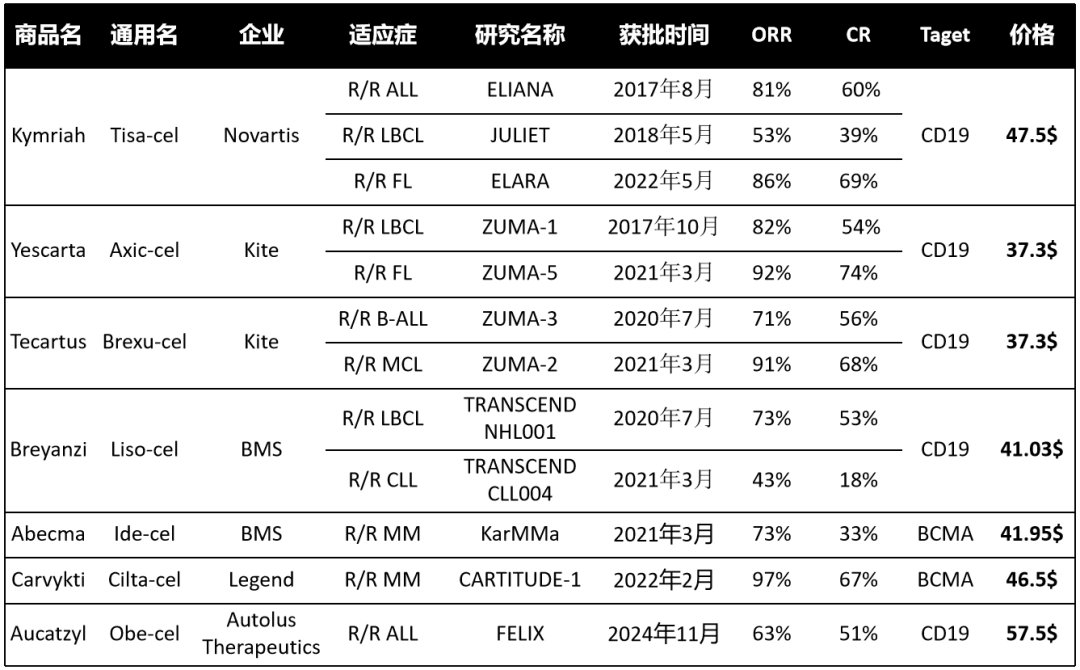
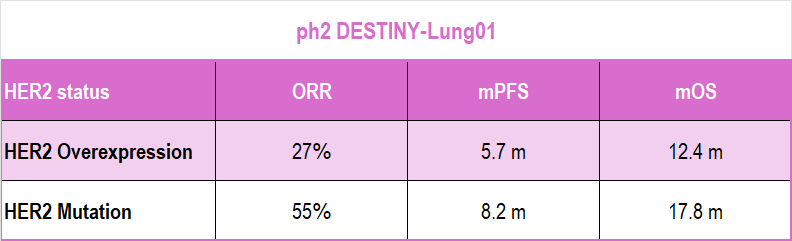
自2000年首个ADC药物获批以来,截至2023年底,美国FDA已批准13款ADC药物上市,同时至少有100种ADC处于不同阶段的临床研究中。近年来,以fam-trastuzumab deruxtecan-nxki(Enhertu®)为代表的ADC在多种肿瘤中显示出显著疗效,推动了该领域的快速发展。
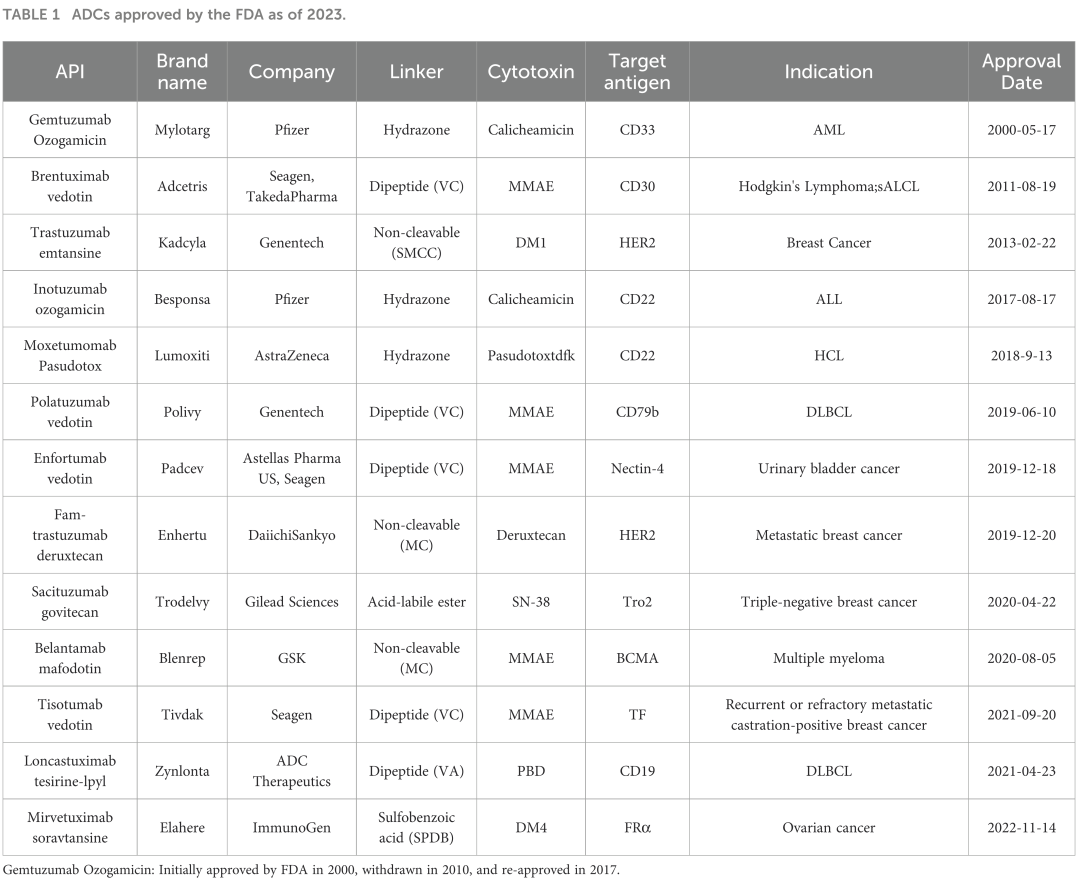
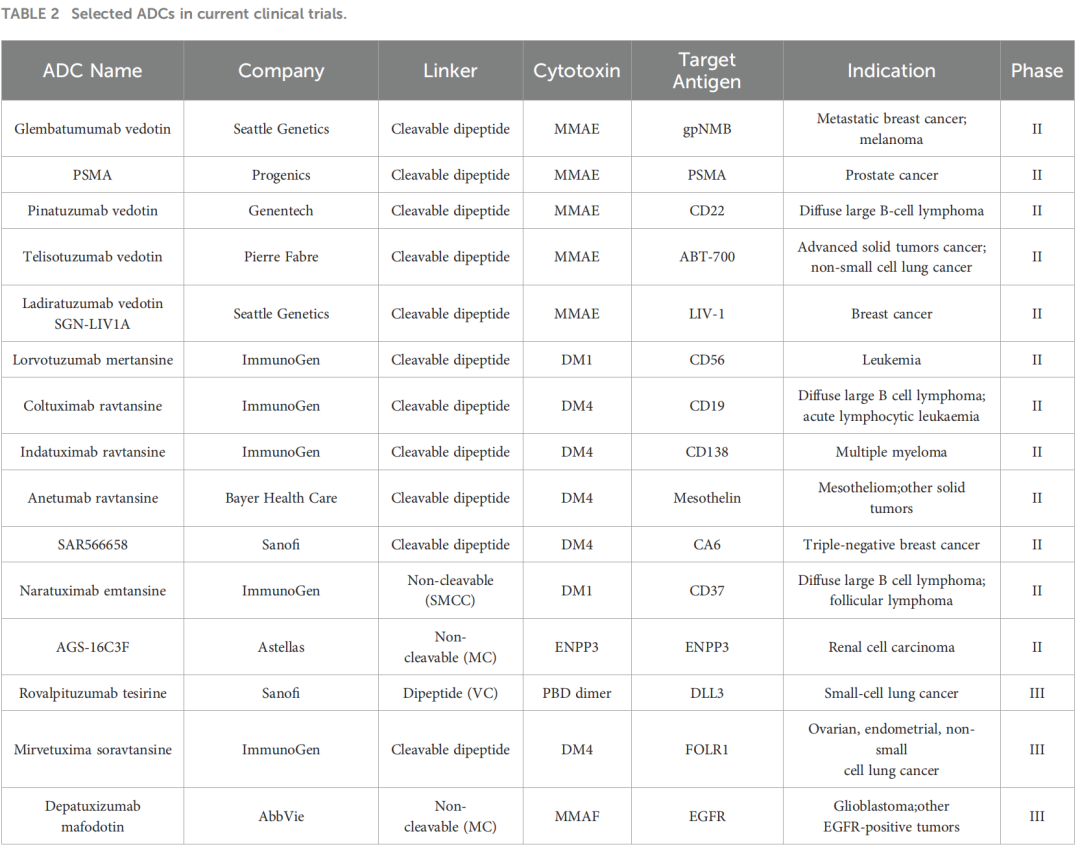
二、ADC的结构组成
ADC的疗效与安全性主要取决于三大组成要素的合理设计与协同作用。
抗体作为靶向递送载体,决定了ADC的靶点选择、体内分布和药代动力学特性。目前临床ADC多采用IgG1亚型抗体,其具有较长半衰期和较低免疫原性。
载荷通常为高效细胞毒性小分子药物,包括微管抑制剂、DNA损伤剂和拓扑异构酶抑制剂。载荷需具备极高的活性,以在有限递送条件下发挥杀伤作用。
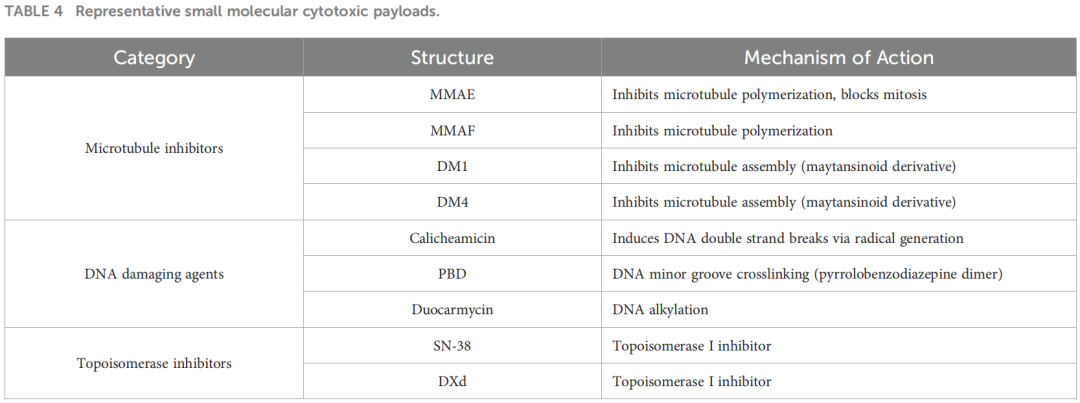
连接体负责在血液循环中维持ADC稳定性,并在肿瘤细胞内实现有效释放。可裂解与不可裂解连接体各具特点,其设计与旁观者效应密切相关。
ADC的复合结构在提高治疗指数的同时,也显著增加了药物设计、生产工艺及质量控制的复杂性。
三、ADC的作用机制
ADC通过抗体与肿瘤细胞表面抗原结合后发生内吞,在溶酶体环境中释放载荷。释放后的载荷通过抑制微管动态或诱导DNA损伤等机制导致肿瘤细胞死亡。部分疏水性载荷可扩散至邻近细胞,产生旁观者效应,从而在一定程度上克服抗原表达异质性。
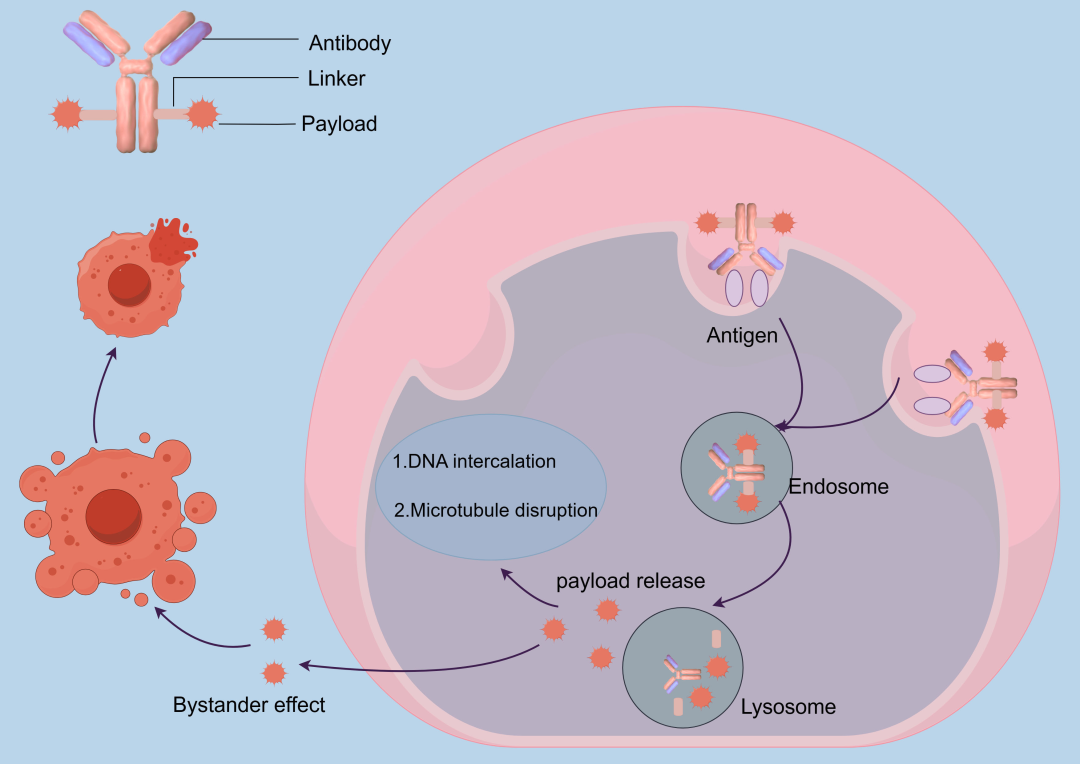
四、ADC面临的主要挑战
尽管抗体偶联药物在肿瘤治疗中取得了显著进展,但其临床开发与应用仍面临一系列复杂挑战。原文从药代动力学、安全性、耐药机制、肿瘤异质性以及生产与转化难度等多个维度,对ADC当前面临的限制进行了系统阐述。
4.1 药代动力学的复杂性
ADC在体内并非以单一形式存在,而是同时包括完整ADC、脱载荷抗体以及游离细胞毒性载荷等多种组分。这种结构复杂性显著增加了其药代动力学研究和临床剂量优化的难度。
ADC在体内的代谢和清除过程受到多种因素影响,包括抗体骨架特性、连接体稳定性、载荷理化性质以及DAR值。载荷或连接体的轻微改变,均可能导致ADC在血液循环中的稳定性发生显著变化。
此外,不同组织和器官对ADC的摄取差异,也可能造成非靶向分布,从而影响安全性和疗效评估。这使得ADC的药代动力学行为往往难以通过单一模型准确预测。
4.2 毒性问题及其来源
毒性是ADC临床开发中最常见且最关键的限制因素之一,约40%的ADC副反应与连接体不稳定或载荷提前释放有关。
ADC毒性主要来源于以下几个方面:
- 靶向相关毒性(target-dependant toxicity):当靶抗原在正常组织中也存在表达时,ADC可能对正常细胞产生杀伤作用
- 非靶向毒性(off-target toxicity):由于连接体不稳定或ADC非特异性摄取,导致载荷在非肿瘤组织中释放
- 系统性毒性:游离载荷进入血液循环后引发的全身不良反应
原文强调,即使采用高肿瘤特异性抗体,若连接体设计不合理,仍可能因载荷泄漏而导致严重毒性,甚至造成临床试验终止。
4.3 肿瘤异质性对ADC疗效的影响
肿瘤异质性是ADC疗效不稳定的重要原因之一。如在空间层面,不同肿瘤区域内靶抗原表达水平存在显著差异,导致ADC仅能杀伤部分肿瘤细胞;在时间层面,靶抗原表达可能随疾病进展发生变化。

4.4 ADC耐药机制
随着ADC在临床中的应用,耐药问题逐渐显现。原文总结了多种已报道的ADC耐药机制,包括:
- 靶抗原下调或表位遮掩
- ADC内吞过程受阻
- 溶酶体功能异常,影响载荷释放
- 药物外排泵表达上调
尽管组合疗法方案和新一代治疗药物在临床前研究中展现出潜力,但其II期临床试验的验证率仍低于30%, 突出了抗性生物学的认知空白。
4.5 药物结构参数之间的权衡
虽然提高DAR可增加单位抗体递送的载荷数量,但同时也会增加疏水性,导致ADC聚集、非特异性结合增强以及体内清除加快。因此,DAR的优化需要在疗效与安全性之间取得平衡。
4.6 生产与转化层面的挑战
ADC的生产涉及抗体表达、化学偶联、纯化及质量控制等多个环节,工艺复杂且对一致性要求极高。这些技术障碍导致每种获批ADC的开发成本超过5亿美元,关键生产挑战包括在批次变异度±5%范围内维持结合效率,以及确保冻干过程中有效载荷的稳定性。
4.7 靶点同质化问题
目前ADC研发中存在明显的靶点同质化现象。已获批及处于临床阶段的多数ADC集中靶向少数肿瘤相关抗原,其中43%的临床候选药物靶向HER2 和 TROP2。
这种靶点集中化一方面源于符合ADC开发要求的理想靶抗原数量有限,另一方面也反映了研发过程中对已验证靶点的重复利用。原文强调,靶点同质化可能在一定程度上限制ADC在更多肿瘤类型中的应用范围。
此外,针对同一靶点开发的多种ADC,尽管在载荷和连接体设计上存在差异,但仍可能面临疗效差异有限的问题。
五、ADC的未来发展方向
5.1 ADC组成要素的改进
5.1.1 抗体的优化方向
抗体的选择和工程化改造是ADC开发的关键因素。人源化和全人源单克隆抗体因其低免疫原性、较长半衰期和良好的免疫效应,已成为ADC开发中最常用的抗体形式。
然而,多个成功ADC靶点(如HER2、TROP2)在部分正常组织中亦存在表达,可能引发靶向相关毒性,甚至导致临床试验中断。为降低此类风险,研究者可采用多种抗体工程策略:
- 抗体结构截短(truncation):去除非必需结构域
- 抗体剪切(clipping):对特定区域进行受控蛋白水解
- Fc结构域修饰:减少Fc介导的非特异性摄取
5.1.2 载荷的拓展与创新
在传统高细胞毒性载荷之外,原文重点强调了新型载荷类型在ADC研究中的兴起。
一类重要方向是免疫调节型载荷,将免疫调节分子作为载荷,通过ADC递送至肿瘤微环境,以增强局部免疫反应。
另一重要方向是靶向蛋白降解剂,包括分子胶和PROTAC类分子。这类载荷通过诱导靶蛋白泛素化和降解发挥作用,与传统细胞毒性载荷在作用机制上存在本质差异。
原文还强调了载荷疏水性对ADC性能的影响。高度疏水的载荷有助于产生旁观者效应,减少与正常组织的非特异性相互作用,减轻聚集形成、快速清除等副作用。为此,引入PEG或多谷氨酸等疏水性屏蔽基团被认为是一种有效的改进策略。
5.1.3 连接体的精细化设计
连接体的设计被认为是提高ADC疗效和安全性的关键因素之一。传统随机偶联方式易导致产物异质性,从而影响药代动力学一致性。
为解决这一问题,位点特异性偶联技术得到广泛关注,包括:
此外,原文介绍了多种新型连接体策略,如树枝状二聚连接体、高DAR连接体,以及溶酶体酶可裂解连接体。这些设计旨在提高ADC在体内的稳定性,并确保载荷在肿瘤细胞内精准释放。
5.2 新型ADC构型
5.2.1 双表位与双特异性ADC
双表位ADC可同时识别同一抗原的不同表位,提高结合稳定性和内吞效率。双特异性ADC则可同时靶向两种不同抗原,用以应对单靶点ADC的耐药问题。
原文列举了多种处于临床前和早期研究阶段的双特异性ADC实例,并指出该策略有助于改善低表达靶点的递送效率。
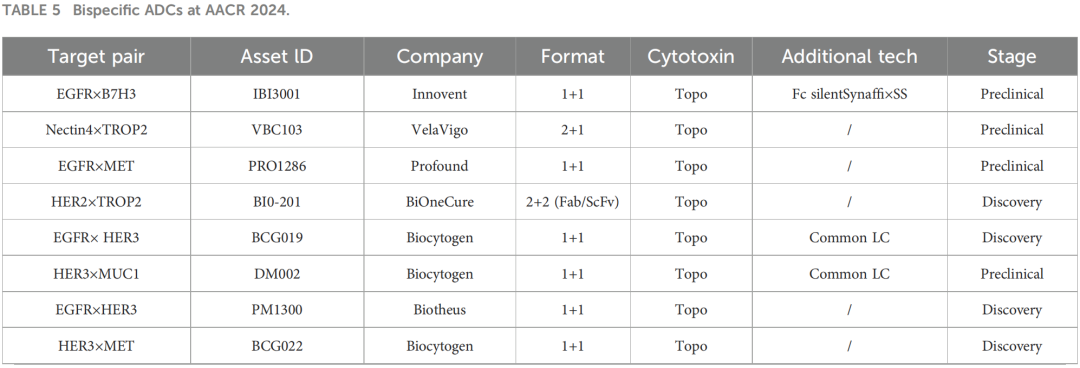
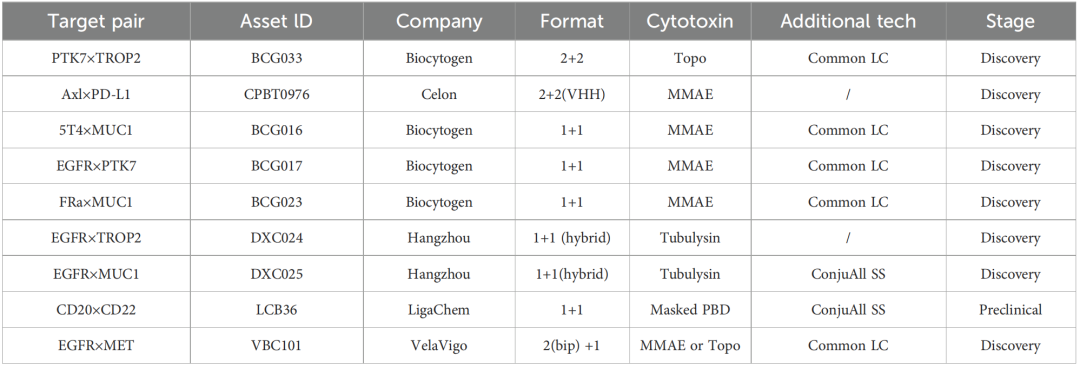
5.2.2 Probody-drug conjugate
Probody-drug conjugate是一类条件激活型ADC,其抗体在正常组织中被屏蔽,仅在肿瘤微环境中经蛋白酶切割后恢复活性。
该构型由三部分组成:抗体、掩蔽肽和可裂解连接肽。其设计理念在于利用肿瘤组织与正常组织之间蛋白酶活性和pH环境的差异,降低正常组织毒性。
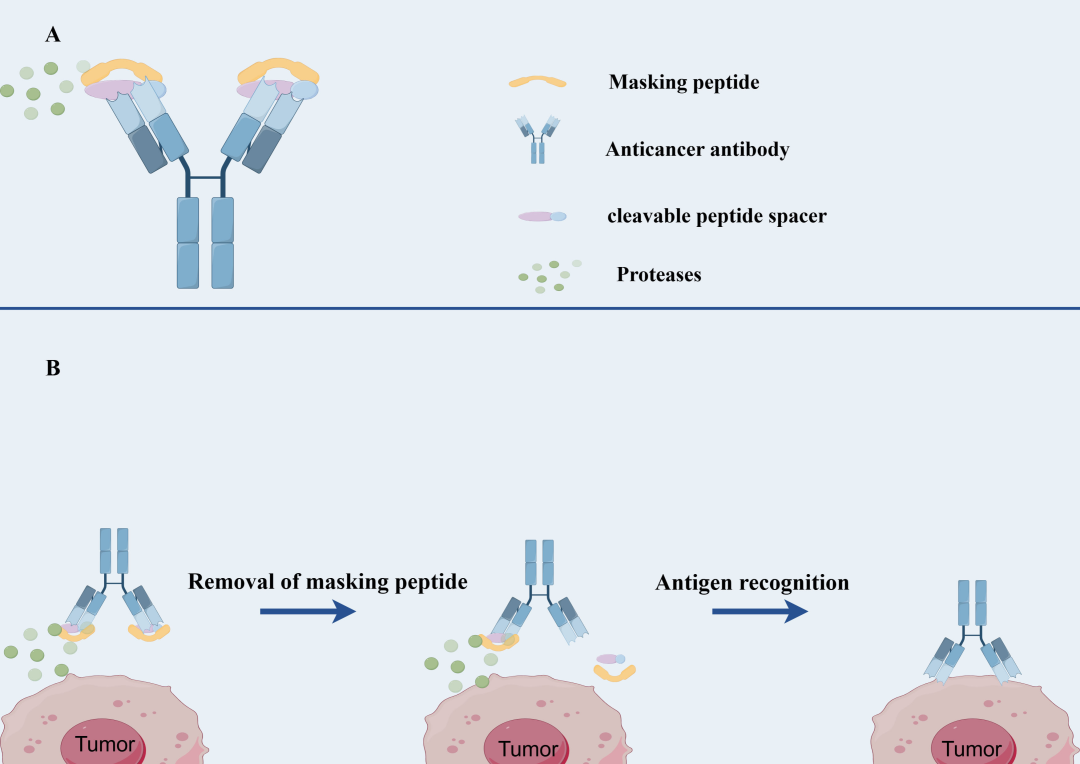
原文介绍了多种处于临床前或早期临床阶段的Probody-ADC实例,并指出该策略具有广泛适用性。
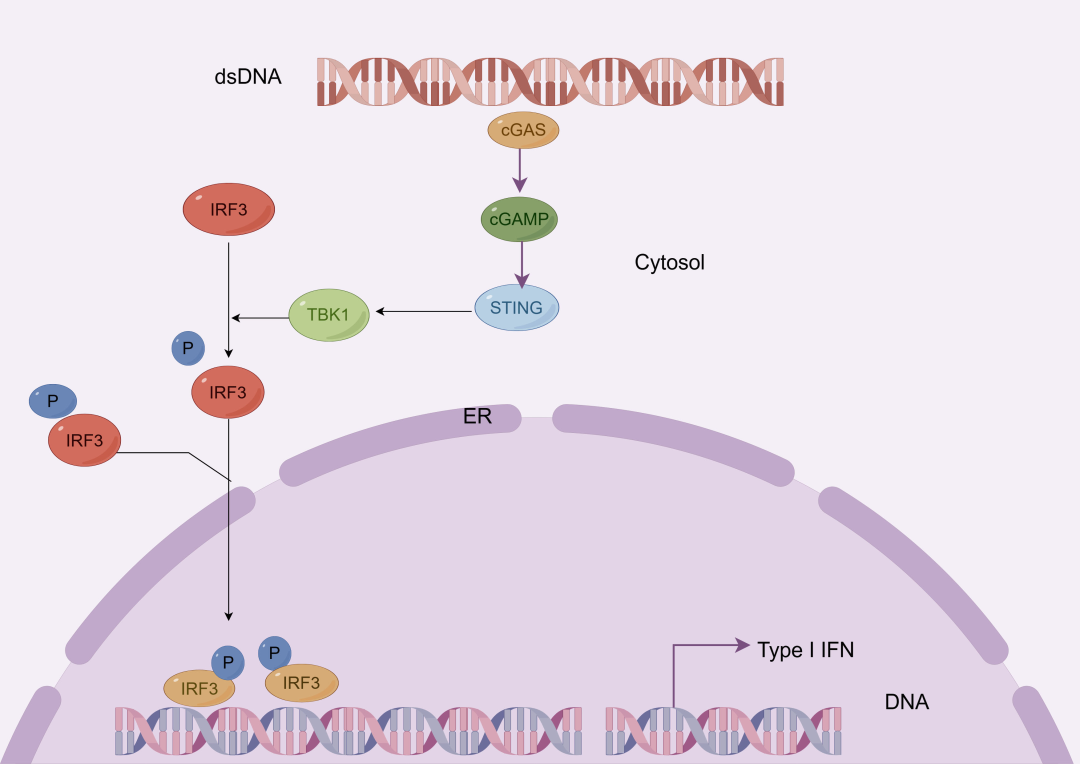
5.2.3 免疫刺激型ADC
免疫刺激型ADC通过将TLR7/8或STING激动剂递送至肿瘤微环境,激活先天免疫并增强适应性免疫反应。