本文来源于微信公众: 医药魔方Pro
近期,科学家们在阿尔茨海默病(AD)治疗方面连获突破。与3月4日中国科学家在Cell杂志首次发表新型靶向蛋白降解技术SPYTAC相隔一天,来自华盛顿大学医学院的一个研究团队在Science发表了首创疗法——CAR-A,单次注射在小鼠中取得了良好的治疗效果。
阿尔茨海默病(AD)是全球范围内导致年龄相关性痴呆的最常见原因,其病理过程始于细胞外的β-淀粉样蛋白(Aβ)的积累,进而发展为神经元内的tau蛋白病变,最终导致神经退行性病变。目前,减缓 AD 进展最有效的策略是使用Aβ 单抗。然而,这类药物存在一些局限性,包括需要高剂量和重复给药(每月一次或两次)、治疗窗口狭窄、诸如淀粉样蛋白相关影像学异常等风险,以及对 Fc 受体γ亚基(FcRγ)信号的依赖。这些挑战凸显了开发新的治疗方法的必要性。
在这项新研究中,科学家们开发的CAR-A疗法只需注射一次就能防止小鼠体内淀粉样斑块的形成(在斑块开始形成之前接受治疗)。此外,对已经出现斑块的小鼠进行一次治疗,就能使淀粉样蛋白斑块的数量减少了一半。
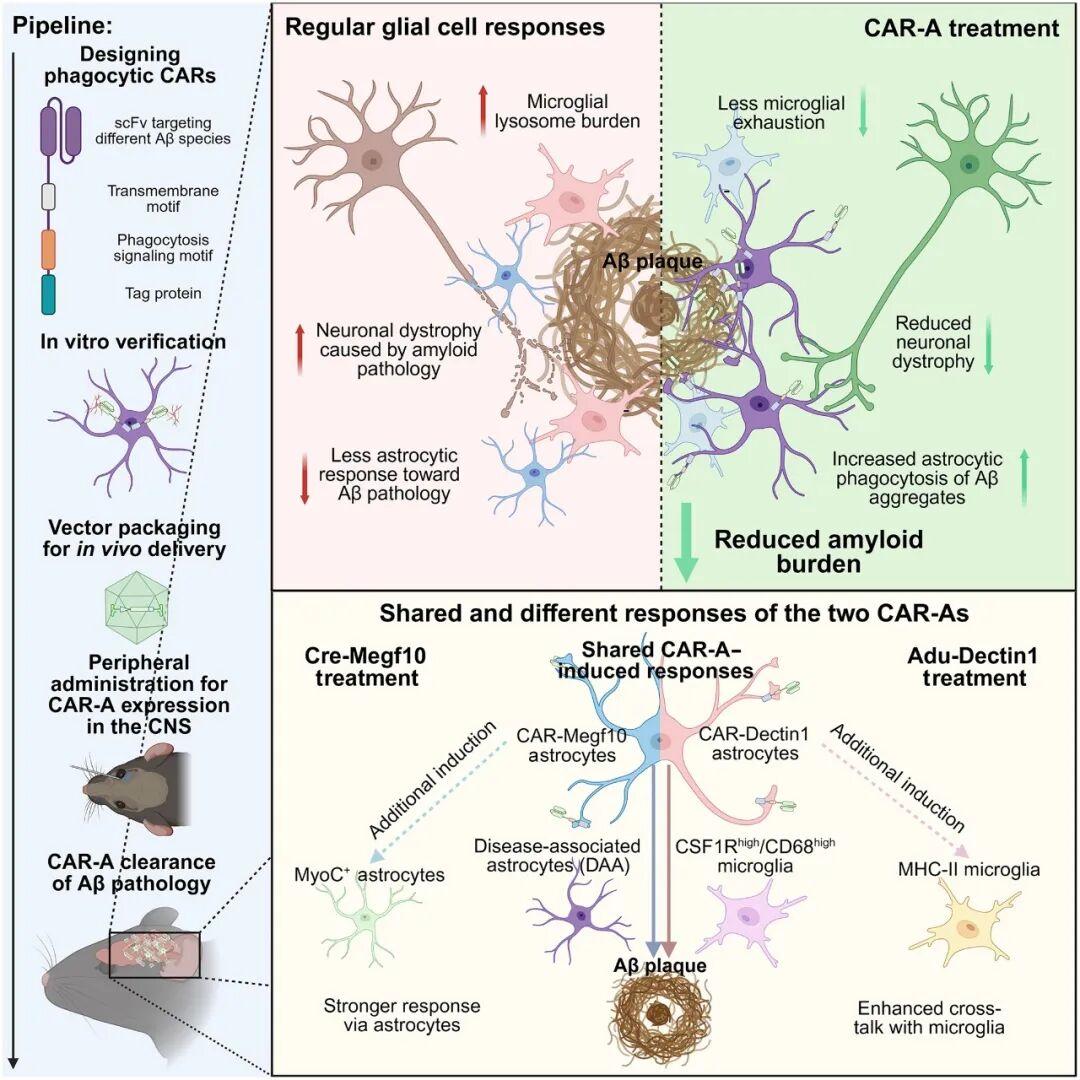
CAR-A 技术在阿尔茨海默病相关模型中对淀粉样蛋白病变的治疗应用(来源:Science)
CAR-A疗法与用于癌症治疗的 CAR-T 疗法类似,后者是将T细胞经改造后表达嵌合抗原受体(CAR)以识别和杀伤癌细胞,而CAR-A疗法“改造”的则是星形胶质细胞(astrocytes),使其能够清除大脑中那些导致认知能力下降的有害蛋白质。
小胶质细胞是存在于大脑中的免疫细胞,它们负责清除大脑中的“废物”,但在神经退行性疾病的情况下,如果受到过度刺激,这些细胞可能会出现功能障碍。为了减轻小胶质细胞的清洁负担,研究人员将大脑中数量最多的细胞类型——星形胶质细胞,改造成了能够清除淀粉样蛋白的“机器”——通过腺相关病毒(AAV)对星形胶质细胞进行基因改造,使其能够表达抗 Aβ 抗体的单链可变区(scFv),并将其与吞噬受体的细胞内结构域相融合(通过AAV-PHP.eB-GFAP体内递送CAR到中枢神经系统中的星形胶质细胞中)。
携带会增加患阿尔茨海默病风险的基因突变的小鼠,在出生六个月后就会在大脑中形成大量的β-淀粉样蛋白斑块。研究人员给两组AD小鼠模型注射了携带CAR表达基因的病毒:一组在小鼠形成斑块前注射,一组在斑块在大脑中聚集后注射。之后,他们等待了3个月。
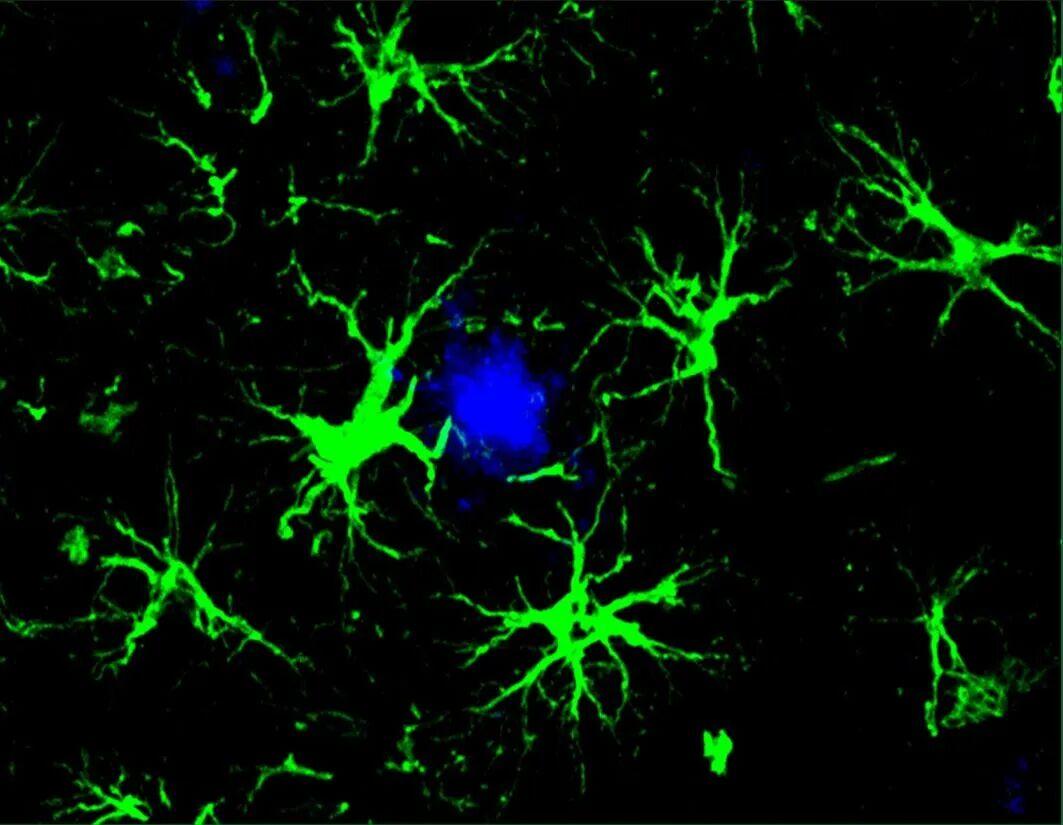
CAR-A疗法(绿色)成功地降低了小鼠大脑中有害的β-淀粉样蛋白斑块(蓝色部分)的数量(来源:Yun Chen,WashU Medicine)
分析结果显示,在第一组更年轻的小鼠中,CAR-A疗法能够阻止β-淀粉样蛋白斑块的形成。在接近6个月大时(此时未经治疗的小鼠的大脑通常已经充满了有害的斑块),接受治疗的小鼠大脑中无斑块形成。与此同时,对于治疗时大脑中已布满斑块的小鼠,接受CAR-A治疗后相较对照组(注射了未携带CAR基因的“空病毒”)β-淀粉样蛋白斑块减少了 50%。
据悉,基于该研究中的重要发现,科学家们已经申请了一项CAR-A关于相关专利。在未来的研究中,他们将继续改进CAR-A疗法,通过微调其设计,以更精准地靶向有害蛋白,同时确保对正常脑细胞功能不会产生不良影响。此外,通过调整CAR使其识别脑瘤上的特异性标志物,有望直接杀伤肿瘤细胞。
“这项研究标志着首次成功实现了对星形胶质细胞的基因改造,使其能够特异性靶向并清除阿尔茨海默病小鼠大脑中的β-淀粉样蛋白斑块。尽管还需要进行更多工作来优化这类疗法并解决潜在的副作用问题,但这些结果为将 CAR-A疗法开发为神经退行性疾病乃至脑瘤的免疫疗法开辟了一个令人兴奋的新机遇。” 领导该研究的Marco Colonna教授说道。