文章来源公众号:爱迪尔笔记 作者:CGTreview
一、in vivo CAR T的核心设计策略
靶向递送系统
载体类型:采用慢病毒载体(lentiviral vector),但通过多重工程化改造克服天然局限:
病毒膜过表达CD47("别吃我"信号),抑制单核吞噬系统清除。
嵌入抗T细胞受体(TCR)纳米抗体,实现T细胞特异性靶向。
免疫原性控制:敲除主要组织相容性复合体I类(MHC-I)基因,降低宿主免疫识别风险。
CAR结构设计
靶向域:人源化抗BCMA单域抗体(VHH)纳米抗体Nanobody。
结构域:人CD8铰链/跨膜区+ 4-1BB共刺激域 + CD3ζ激活域。
调控元件:上游含T细胞特异性合成启动子(专利号CN109134665B),限制CAR表达于T细胞。
二、制造流程的革命性简化

关键突破:消除复杂体外制造流程,显著缩短治疗等待时间,降低生产成本。
三、临床验证与挑战
安全性
急性炎症反应:所有患者输注后24h内出现CRS(3例3级,1例1级),伴随细胞因子(IL-6、IL-10)双峰释放。
神经毒性:1例发生1级ICANS(与高CSF肿瘤负荷相关)。
血液学毒性:3-4级中性粒细胞/淋巴细胞减少(均恢复至基线)。
应对措施:地塞米松预给药有效控制CRS/ICANS。
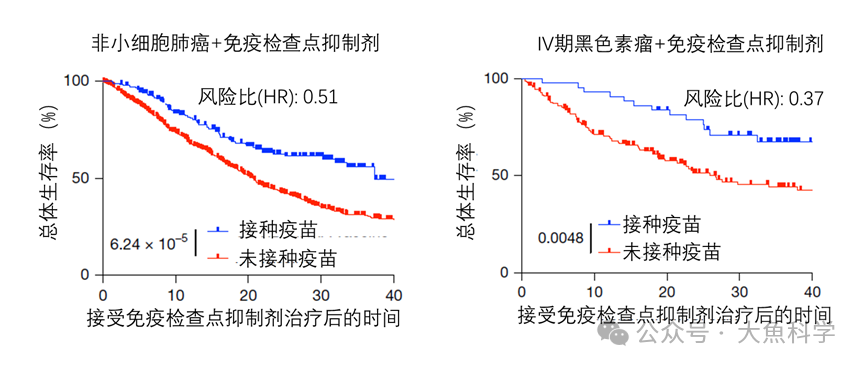
疗效初步证据
肿瘤清除:2例达严格完全缓解(sCR),2例部分缓解(PR),包括髓外病变消退。
CAR T扩增动力学:外周血CAR T细胞4-8天可检出,10-17天达峰,并浸润骨髓/肿瘤/CSF。

机制探索
肿瘤微环境重塑:活检显示CD3+ T细胞浸润增加,BCMA+肿瘤细胞减少。
CAR T表型:中央记忆型CAR T(Tcm)占比高者扩增更佳(如Patient 1)。
四、局限性与未来方向
脱靶风险:虽未在CD3⁻淋巴细胞/NK细胞中检测到高CAR表达,但需长期监测造血细胞转导。
剂量优化:起始剂量(2×10⁹ TU)仅为非人灵长类试验剂量的1/10,疗效潜力可能被低估。
临床证据:需扩大队列、延长随访(持久性验证)及随机对照试验。
总结
ESO-T01通过靶向性慢病毒载体设计(T细胞特异递送+免疫屏蔽)和体内重编程策略,首次实现免制造流程的in vivo BCMA CAR T治疗。其突破性在于将传统CAR T的定制化疗法转化为即用型产品,为复发/难治性骨髓瘤提供高效、可及的新选择,但安全性管理(如CRS)及长期风险仍需深入探索。
Key Take away
·技术来源于比利时EsoBiotec, Mont-Saint-Guibert, Belgium;
·慢病毒+nanobody,慢病毒载体容量小,nanobody刚好可以克服。