文章来源公众号:终不似少年游 作者:闻李
本来想找篇最新的、集齐当前最火热的TPD领域企业研发管线的汇总文章,找了一下没找到合适的,只能自己整理下,目的是想追踪TPD行业管线/靶点的变动。当然,仅聚焦在UPS系统(ubiquitin–proteasome system)的PROTAC和分子胶两大块,其他非UPS技术种类很多,但暂时还未成主流。PROTAC主要罗列四小龙的Arvinas、Kymera、C4和Nurix,分子胶领域则选择Monte Rosa。
Arvinas是当之无愧PROTAC技术先驱。2025 年 6 月 6 日,Arvinas宣布与其合作伙伴辉瑞一起,为其PROTAC药物Vepdegestrant(ARV-471)向FDA提交NDA,用于治疗既往接受过内分泌疗法的ER阳性/ HER-2阴性、ESR1 突变的晚期或转移性乳腺癌患者。本次提交基于 VERITAC-2 (NCT05654623) 的结果。作为首个提交上市申请的PROTAC药物,Vepdegestrant在其VERITAC-2三期临床中与23年前获批上市的SERD氟维司群(Fulvestrant)的头对头比较并没有获得众望所归的结果,在对CDK4/6抑制剂和内分泌疗法耐药的ER+/HER2-转移性乳腺癌患者中,仅在ESR1突变人群中达到了PFS主要终点,而在ITT人群中,mPFS未能显示出统计学上的显著改善(ER野生型患者未能获益),mOS数据暂未成熟。这一消息的公布也直接导致Arvinas的股价暴跌及裁员,最近CEO John Houston也将会退休离任。作为合作方的辉瑞,也选择对Vepdegestrant战略收缩,终止一线联合CDK4抑制剂Atirmociclib的关键试验。
Arvinas最新管线中靶点包括ER、BCL6、LRRK2、KRAS G12D以及许可给诺华的ARV-766的AR;适应症为肿瘤和神经学领域疾病。 Kymera作为PROTAC四小龙之一,发展也是相当凌厉。STAT6 PROTAC药物KT-621近期公布的一期临床中,在健康人中获得与Dupilumab相比积极的阳性结果,虽然同一时间合作方赛诺菲宣布放弃开发一代IRAK4 PROTAC药物KT-474,但同时也决定转而开发二代同靶点的KT-485。Kymera宣称KT-485的选择性和活性更强,也没有KT-474带有的QTc延长信号。最新管线中靶点包括STAT6、IRF5、IRAK4以及和吉利德合作的CDK2;靶点和适应症大部分属于当下最火热的免疫学范畴。 Nurix的管线丰富,肿瘤和I&I领域都有布局,肿瘤靶点集中在BTK、BTK-IKZF、CBL-B、Pan-mutant BRAF,I&I靶点则包括BTK、IRAK4、STAT6(同Kymera);从Modality看,Nurix还布局了DAC,还比较早期。 C4的靶点选择相比Arvinas、Kymera和Nurix,似乎更为保守一些,包括一代分子胶沙利度胺(Thalomid)的靶点IKZF1/3,,以及EGFR L858R、BRAF V600突变。 Monte Rosa是分子胶领域的先行者,其核心竞争力在于其QuEEN平台,该平台整合了人工智能、蛋白质组学和高通量筛选技术,能够系统性挖掘分子胶的新靶点和作用机制。Monte Rosa的靶点布局包括VAV1(许可给诺华)、NEK7、GSPT1、CCNE1/CDK2,领域涵盖I&I和肿瘤。 比较有意思的是NEK7靶点:异常的NLRP3(NACHT-, leucine-rich repeat [LRR]- and pyrin domain [PYD]- containing protein 3)炎症小体激活与多种炎症疾病相关;研究表明,NIMA-related kinase 7(NEK7)通过桥接相邻的NLRP3亚基来介导NLRP3炎症小体的组装和激活。因此,减少NEK7蛋白可能会阻断NLRP3的激活。但合作方诺华最近发表了篇临床前研究文章,公布其开发的NEK7靶点分子胶NK7-902,对NEK7的降解导致的IL-1β抑制并不完全且短暂,认为NEK7并非NLRP3激活所必需,在缺乏NEK7的情况下,可能存在其他因子替代NEK7或对其进行补偿。所以NEK7是否能成为一个理想的靶点,需要Monte Rosa的临床数据去验证。
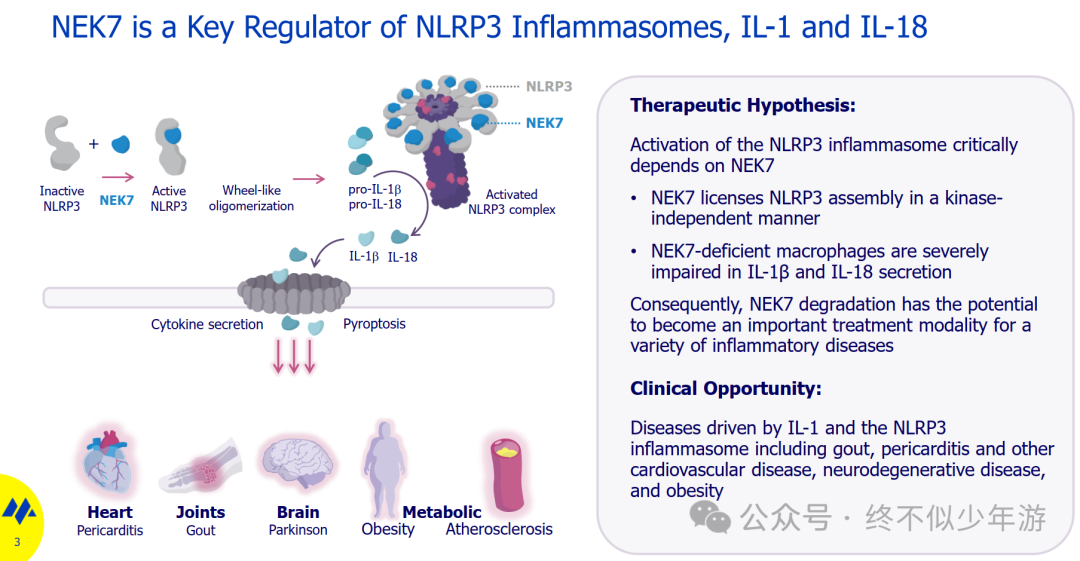
另外,2025 年 7 月,Monte Rosa在《Science》上发表文章,揭示了 CRBN 型分子胶识别底物蛋白的三种全新机制,突破了传统认知中分子胶仅靶向含 G 环结构蛋白的限制。研究证实,泊马度胺等CRBN分子胶降解剂可通过G-环或含甘氨酸的β-发夹结构(G-loop or glycine containing β-hairpin)的结构降解子(structural degron)结合其靶点。包括上述诺华的文章中,对NEK7的分析显示,其存在一个β-发夹结构降解子(β-hairpin structural degron,NEK7第51-60位氨基酸),与酪蛋白激酶1α(CK1α)的β-发夹结构高度相似(均方根偏差[RMSD]为0.25 Å),表明NEK7可能成为CRBN分子胶的靶点。