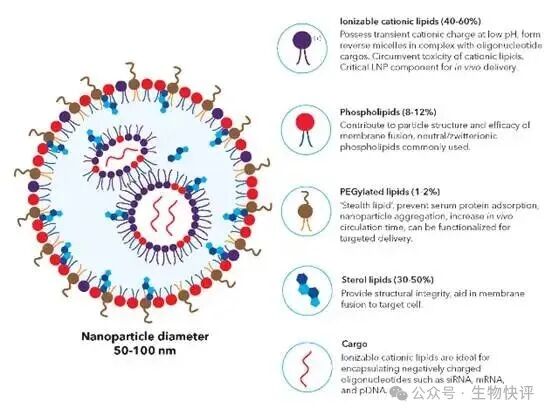
核酸,这一名词已经家喻户晓,尤其在接种新冠疫苗的现场发现核酸残留,曾一度引起恐慌,随着研究及取样调查的深入,人们了解了产生阳性的原因,同时对生物制品的核酸残留也有了一定的认识。用于疾病治疗或预防的生物制品有着严格的质量控制,其中核酸残留是各项质控标准的重中之重。
生物制品的核酸残留具有潜在的危害性。生物制品的宿主细胞大多是连续传代细胞,拥有无限增殖的能力。残留的宿主细胞核酸可能会在人体内造成细胞增殖失控,变为肿瘤细胞。核酸残留可能存在感染性病毒基因,增加体内免疫反应。因此,从生物制品安全角度和科研需求,进行有效的核酸残留去除,是非常重要的。
我国参照WHO、FDA和欧盟标准,在药典中对生物制品的核酸残留量有明确规定。生物制品的核酸残留主要集中在重组蛋白、抗体及疫苗的大规模纯化及生产过程。药典规定要求酵母、大肠杆菌表达的生物制品中DNA残留量不超过10ng/剂,CHO和Vero细胞表达的EPO、狂犬疫苗、乙肝疫苗等不超过100或10pg/剂。
在一般的情况下,含氯消毒液、紫外灯照射等能够消除环境或产品表面的核酸,但是对于生物制品在生产过程中产生的核酸,就需要专业的核酸去除剂了。现在大多选择核酸酶进行去除。核酸酶能够消除核酸残留的潜在危害,降低样品粘度,提高产品纯化效率。
Pannarase是一种来自于粘质沙雷氏菌(Serratia marcescens),经基因工程改造的核酸内切酶。Pannarase高活性地降解各种类型的DNA和RNA,包括双链、单链、线状、环状等,将核酸降解成3~5个碱基长度的5’-单磷酸寡核苷酸,所以又被称为“全能核酸酶”。
一,逐典Pannarase全能核酸酶优势
1.GMP条件生产 高比酶活 无动物源
2.高效核酸降解力
3.高质控标准 严格内毒素控制
4.无His标签,无氨苄青霉素
1.全能核酸酶应用条件
全能核酸酶的酶活会受到多种因素的影响(例如温度、pH、离子强度等),故用量范围也会从0.1 U/mL-250 U/mL不等。因此,不同的操作环境下酶的最佳浓度不同,需要通过实验设置梯度进行最佳条件的摸索。
应用实例:
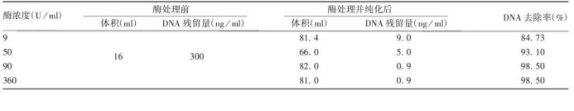
样品:狂犬病毒浓缩液
处理条件:核酸酶浓度50~90U/ml ,
37 ℃处理 2 h,转入18 ~ 26 ℃处理 6h

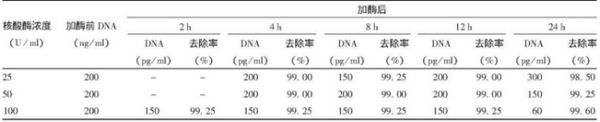
样品:狂犬病病毒浓缩液
处理条件:25、50和100 U/ml,37℃

样品:流感病毒浓缩液
处理条件:10 U/mL,37℃