本文来源于微信公众: 和光再生-外泌体囊泡-衰老 作者: Alvin4th
体外自体CAR-T疗法的价值显而易见:对于某些患者而言,这些疗法提供了重生的机会。然而,这种方法也存在诸多局限性。患者与医生之间的就诊流程复杂,且由于需要在符合GMP规范的条件下对每位患者经血细胞分离术获得的T细胞进行体外操作,因此生产成本高昂且物流要求苛刻。
接受治疗的患者人数仅占需要治疗患者的一小部分,这限制了这项突破性疗法的普及。作为现成产品销售的体内CAR-T疗法能否打破这些障碍,扩大患者的可及性?
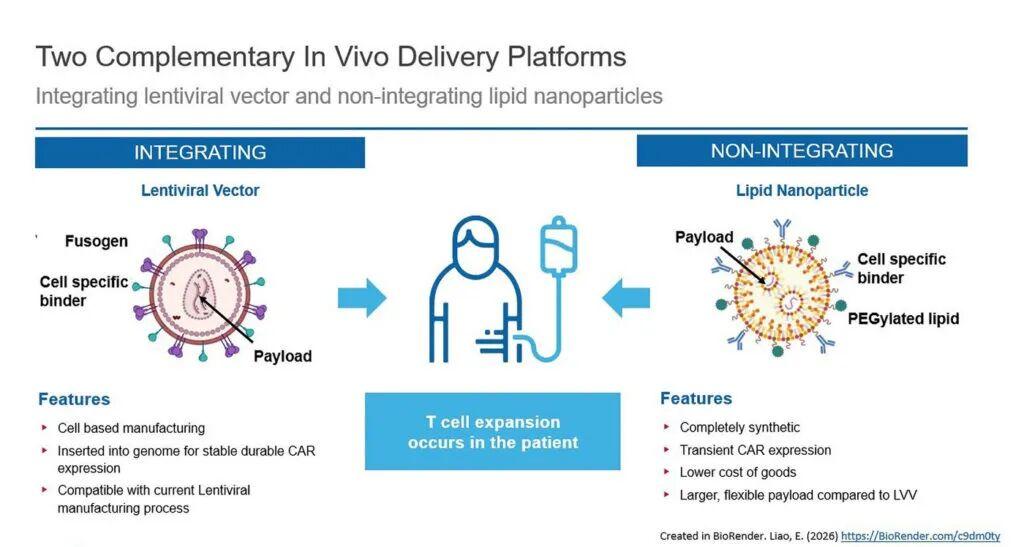
目前正在研究多种体内CAR-T细胞治疗平台,包括整合型和非整合型。整合型平台通常依赖于病毒载体,例如慢病毒,类似于大多数已获批准的CAR-T疗法中使用的载体。与其他病毒基因治疗策略一样,这些平台也存在已知的风险,包括插入突变的可能性。
尽管存在这些风险,早期临床数据表明体内CAR-T疗法具有显著潜力。两项早期研究——一项由比利时EsoBiotec公司与中国深圳普瑞金生物制药公司合作开展,另一项由波士顿Kelonia Therapeutics公司开展——均已证实,使用慢病毒载体可清除多发性骨髓瘤的肿瘤细胞。
互补的非整合平台采用多种递送方法,包括脂质纳米颗粒(LNP)、纳米囊泡和外泌体。在这些情况下,作为主要递送载体的mRNA的半衰期是一个挑战,可能需要具备在不引起免疫原性的情况下重复给药的能力。基于DNA的有效载荷正被研究作为替代方案。
各大制药公司正竞相收购体内细胞工程平台,这表明体内细胞重编程正成为治疗策略的核心支柱。一波公司并购浪潮预示着这一新兴但发展迅速的领域即将从肿瘤学应用扩展到其他疾病领域,例如自身免疫性疾病。
具体性和规模化挑战
2021年初,赛诺菲看到了这一潜力,并收购了Tidal Therapeutics公司。当时,赛诺菲预期这种新一代的即用型CAR-T细胞疗法有望使更广泛的患者群体受益。
赛诺菲副总裁兼全球基因组医学负责人Christian Mueller博士表示:“为了提高效率,我们正在研究非整合式方法,旨在将mRNA载体靶向递送至特定细胞类型。” 赛诺菲的CD8靶向脂质纳米颗粒(LNP)能够高效地将CD19 CAR mRNA递送至CD8 T细胞。
这种可电离脂质及其制剂能够高效地在体外和动物模型中转染T细胞。在非人灵长类动物(NHP)研究中,靶向脂质纳米颗粒(LNP)的给药可显著且持续地清除B细胞,且仅伴有少量、大多短暂的亚临床副作用。
“我们对靶向基团进行工程设计,以确保其在特定位点进行脂化修饰,从而将其整合到脂质纳米颗粒(LNP)中,”穆勒解释道。这种位点特异性修饰保证了批次间的一致性,并且相对于其他LNP靶向方法而言,具有更强的可扩展性。
规模化生产可能面临挑战。靶向脂质纳米颗粒(LNP)需要制备多种不同的组分,例如mRNA、脂质和靶向配体,所有这些组分都需要配制成成分一致的药物产品。赛诺菲在工程技术方面的重大突破,使得高效的靶向LNP生产工艺成为可能。
穆勒预测,CAR在体内的表达持久性将持续提高。目前存在多种策略,包括利用脂质纳米颗粒(LNP)介导的DNA递送来延长给药窗口,甚至通过基因插入技术实现CAR的永久表达。未来几年的持续研发工作将揭示这些先进有效载荷在不同应用中的适用性。
CAR-T细胞及其靶点的应用范围将持续拓展,超越血液学领域。基因工程有望构建更复杂的回路,从而充分发挥体内细胞重编程的潜力,包括但不限于表达特定因子以治疗实体瘤。
赛诺菲正在考虑将其靶向LNP平台的应用范围从体内CAR-T细胞疗法扩展到其他细胞类型的重编程。特别是,靶向造血干细胞的研究颇具前景,有望为患者带来潜在的治愈性疗法。
收购活动加速进行
近年来,行业并购活动加速进行。据《肿瘤治疗产品线》(Oncology Pipeline)报道,2025年,百时美施贵宝(BMS)以15亿美元收购了Orbital Therapeutics及其基于RNA的体内治疗产品线。吉利德通过其子公司Kite,承诺向中国细胞治疗专家普瑞根(Pregene)支付1.2亿美元的首付款,并根据里程碑事件支付最高15亿美元的款项,随后又收购了Interius BioTherapeutics。
其他大型制药公司也采取了类似举措。阿斯利康以高达10亿美元的价格收购了EsoBiotec,而艾伯维则因斥资21亿美元收购Capstan Therapeutics以及与Umoja达成另一项许可协议而成为新闻焦点。Kelonia Therapeutics也宣布与强生公司开展战略合作,以推进新型体内CAR-T细胞疗法的研发。
利用平台经验
2020年代技术和平台的发展速度远远超过以往几十年。人工智能赋能的信息获取增强了假设的生成,而来自全球试验网络的循证知识积累则加速了临床开发。
“尽管体内CAR生成仍处于起步阶段,但我们已经看到了巨大的潜力。体外疗法,包括Yescarta®和Tecartus® ,迄今已用于治疗近23,000名患者,这些疗法积累了丰富的经验,便于我们进行比较,从而增强了我们对该方法的信心。”吉利德旗下公司Kite的高级副总裁兼全球研发主管Priti Hegde博士表示,“投资规模巨大,应用前景广阔。如果我们能够成功开发这些平台,将会彻底改变行业格局。”
一个悬而未决的问题是,在没有淋巴清除方案来清除免疫抑制细胞的情况下,CAR 本身是否能够发挥作用,扩增并杀死靶细胞。“我们需要临床数据和长期患者监测,以了解体内疗法是否与体外疗法一样持久,并提供相似的临床特征,”Hegde 强调说。
鉴于在慢病毒体外平台方面的经验,Kite选择使用基于慢病毒的平台进行体内CAR开发工作。为防止非特异性递送,工程化病毒表面包覆有靶向分子,以便将有效载荷特异性地递送至表达靶标的细胞。通过改变靶向结合分子和有效载荷,可以使其适用于不同的细胞类型和疾病,并可用于关键知识产权的构建。
Hegde 指出了规模化生产的关键重要性。“我们投入了大量精力来生产慢病毒。收购 Interius BioTherapeutics 是对我们内部研发工作的有力补充。”
Interius 的病毒载体模块化可扩展模型能够加快项目开发速度。首个在澳大利亚和欧洲开展剂量递增 I 期临床试验的项目,靶向淋巴瘤中的 CD20,并采用一种靶向 T 细胞 CD7 的非激活型结合剂。“现在,生产流程已整合到 Kite Research,我们正在探索其他结合剂和 CAR 构建体,”Hegde 补充道。
采取两种方法
艾伯维目前正在研究体内CAR T 平台在免疫介导疾病和癌症中的应用。
靶向脂质纳米颗粒 (tLNP) 的示意图,该纳米颗粒携带 mRNA 有效载荷,其外部带有靶向结合基团,可将其引导至目标 T 细胞群。“体内CAR-T细胞疗法有望彻底改变我们治疗难治性自身免疫性疾病和癌症的方式,并有可能使我们更接近真正治愈的可能,”艾伯维公司高级副总裁兼全球发现研究负责人乔纳森·塞奇威克博士表示。“该疗法可以克服自体CAR-T疗法的主要障碍,并最终可能有助于扩大CAR-T疗法的受益患者群体。”
一种方法采用Capstan Therapeutics公司最初开发的专有靶向脂质纳米颗粒(tLNP)平台进行RNA递送。tLNP旨在最大限度地减少脱靶效应,包括肝脏脱靶效应。LNP上的靶向结合剂能够识别特定的T细胞表面标志物,从而将RNA递送至目标T细胞群,使其瞬时转化为表达CAR的细胞,这些细胞可以寻找并摧毁已知驱动某些自身免疫性疾病的致病细胞。
据塞奇威克介绍,ABBV-619旨在对患者体内的CD8+ T细胞进行编程,使其表达CD19特异性CAR。通过生成这些表达CD19 CAR的细胞毒性CD8 T细胞,该方法旨在清除外周血和组织中的致病性记忆B细胞,从而使初始B细胞得以重新增殖,最终可能重置免疫系统,阻止或逆转疾病进展。ABBV-619目前正处于治疗B细胞介导的自身免疫性疾病的I期临床试验阶段。
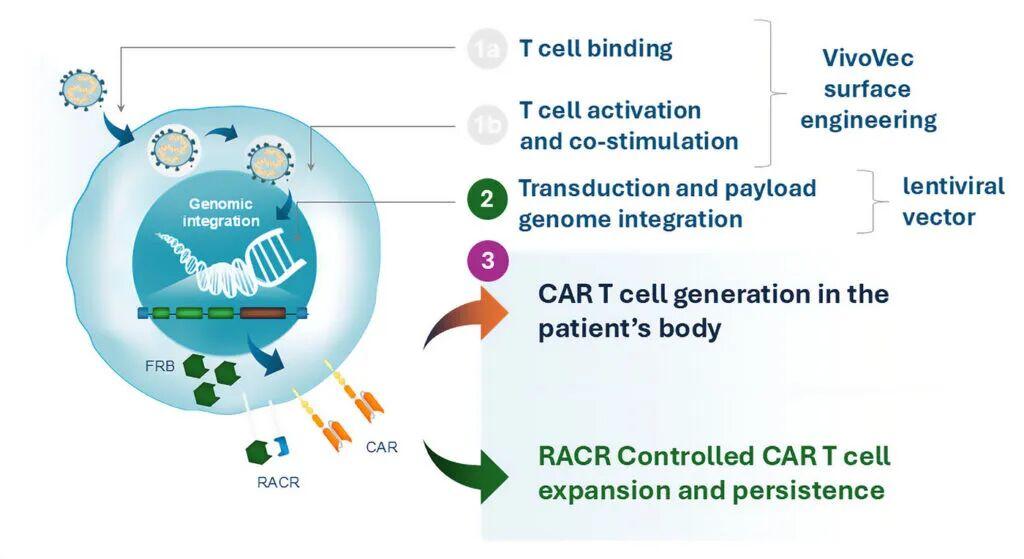
该公司与Umoja的合作利用其专有的VivoVec™平台开发用于肿瘤治疗的体内CAR-T疗法。该平台结合了第三代慢病毒载体基因递送技术和一种新型T细胞靶向激活表面复合物。VivoVec可与RACR(雷帕霉素激活的细胞因子受体)联合使用,从而有望增强VivoVec工程化免疫细胞的存活和扩增。
艾伯维拥有 Umoja 的 CD19 靶向体内CAR T 候选药物的独家授权选择权,其中包括 UB-VV111,这是 Umoja 目前处于 I 期研究阶段的血液恶性肿瘤主要临床项目。“凭借我们在免疫学和肿瘤学领域的深厚底蕴,发挥我们的内部能力,以及战略投资和合作伙伴关系,我们致力于推进体内CAR T 平台的发展,以创造更易于获取、更持久、更具变革性的疗法,从而靶向多种致病细胞类型,”Sedgwick 表示。