本文来源于微信公众: 话药源记 作者: 话药源
前文已述该技术在自免领域的重要进展CD19/CD3 TCE ——从“抗癌”到“免疫重启”。
随着技术的不断突破,TCE 已经从血液瘤的“专属武器”迅速拓展至实体瘤,并在近两年(2025-2026年)历史性地跨界进入了自身免疫性疾病领域,成为目前全球医药圈最具爆发力的赛道之一。
一、TCE技术的作用机制与运用
1. 核心作用机制 (Mechanism of Action)TCE 的本质是“双特异性或多特异性抗体”,它相当于免疫系统的人工“牵线搭桥”者。
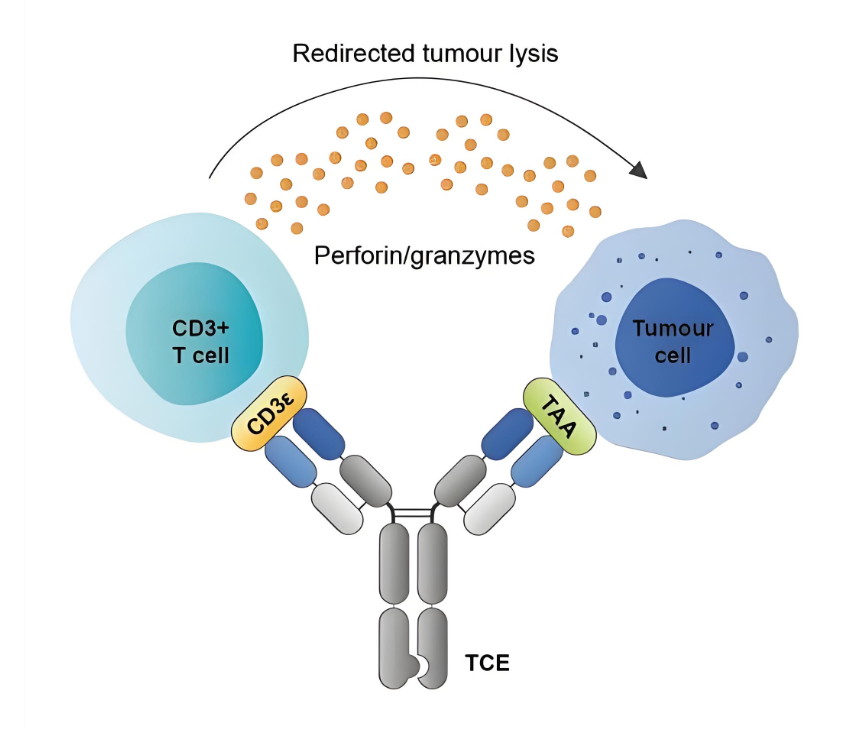
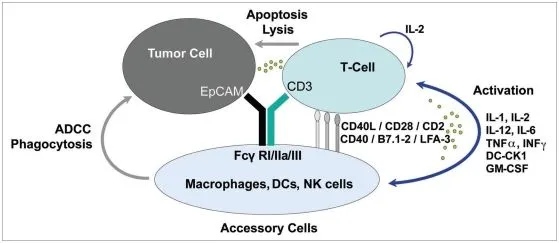
经典机制 (第一代/第二代):TCE 的一端特异性结合肿瘤相关抗原 (TAA,如 CD19, CD20, BCMA, PSMA),另一端结合 T 细胞表面的 CD3 受体。这种设计能够绕过传统的 MHC (主要组织相容性复合体) 限制,强制将 T 细胞拉拽到肿瘤细胞表面形成“免疫突触”,激活 T 细胞释放穿孔素和颗粒酶,直接将靶细胞定向爆破。
下一代演进机制 (第三代 TCE):为了解决传统 TCE 带来的严重毒性(如细胞因子释放综合征 CRS 和中枢神经系统毒性 ICANS),在研技术正向以下方向迭代:前体掩蔽技术 (Masked/Prodrug TCE):利用空间位阻掩盖 CD3 结合域。药物在血液循环中处于“休眠”状态,只有到达肿瘤微环境 (TME) 时,被特异性蛋白酶切割才会“脱去面具”激活杀伤力,极大降低了系统性毒性。双重信号/共刺激技术:除了 CD3(第一信号),引入 CD28 或 4-1BB (CD137) 作为共刺激信号,防止 T 细胞过度耗竭 (Exhaustion),延长杀伤持久性。
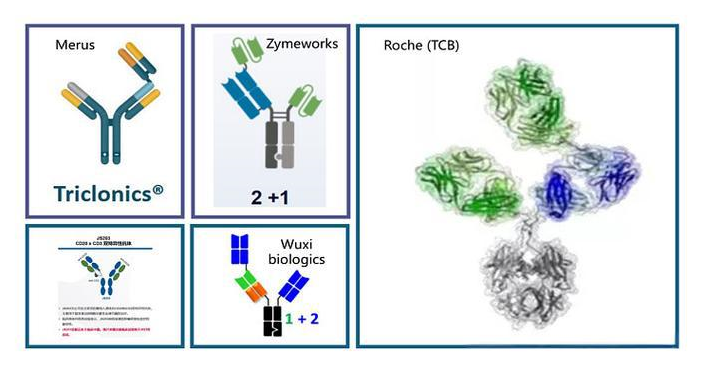
图片来源于雪球
2. 全球临床管线核心进展 (按疾病领域)
目前,TCE 的临床开发呈现出“血液瘤深耕、实体瘤破局、自免异军突起”的三足鼎立态势。
A. 血液肿瘤 (HemOnc) —— 已进入成熟商业化与前线推进期血液瘤是 TCE 最成熟的阵地,重点在于提升用药便捷性(如皮下注射)和向早期治疗线推进。
核心靶点:CD19, CD20, BCMA, GPRC5D。
管线代表:CD20 x CD3:Epcoritamab (AbbVie/Genmab) 和 Glofitamab (罗氏) 已获批用于淋巴瘤,目前正在向一线联合疗法拓展。
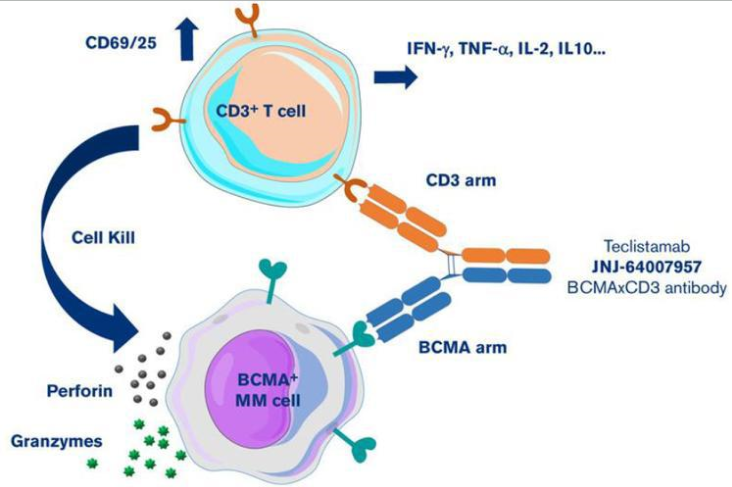
BCMA x CD3:Teclistamab (强生) 和 Elranatamab (辉瑞) 已成为多发性骨髓瘤 (MM) 的标准疗法。
强生的 Talquetamab (GPRC5D 靶点) 也为复发患者提供了新选择。
B. 实体瘤 (Solid Tumors) —— 处于技术破局与适应症爆发期实体瘤存在微环境免疫抑制和靶点“脱靶毒性”问题,但近期迎来了重大突破。
核心靶点:DLL3, PSMA, KLK2, STEAP1, CLDN18.2。
管线代表:
小细胞肺癌 (SCLC):安进的 Tarlatamab (Imdelltra, DLL3 x CD3) 于2024年获批,是实体瘤 TCE 的历史性里程碑。默沙东 (MSD) 收购的 HPN328 (Gocatamig) 目前也在处于二期冲刺阶段。
前列腺癌:强生 Pasritamig (KLK2) 处于临床三期领跑外,安进的 Xaluritamig (STEAP1) 和 Astellas 的 VIR-5500 (掩蔽型 PSMA) 也在快速推进。
消化道肿瘤:安斯泰来 (Astellas) 的 ASP2138 (CLDN18.2 x CD3) 正在胃癌中展现出极具潜力的皮下注射初步疗效数据。
C. 自身免疫性疾病 (Autoimmune) —— 2025/2026年最火爆的新兴赛道医学界发现,利用 CD19 x CD3 的 TCE 来“深度清除”导致自免疾病的致病性 B 细胞,可以达到类似 CAR-T 的长效缓解效果,且具备“现货型 (Off-the-shelf)”的巨大优势。适应症:系统性红斑狼疮 (SLE)、类风湿性关节炎、重症肌无力等。
管线代表:目前大量管线处于 Phase 1 阶段,大药企正在疯狂扫货具有掩蔽技术或低毒性特征的 CD19 TCE 分子。
TCE在自免疾病中的核心机制:
与肿瘤中“持续追杀靶细胞”不同,TCE 在自免中的目标是 “免疫重启 (Immune Reset)”。通过短暂、强效地激活体内现存的 T 细胞,TCE 能迅速且彻底地清空外周血及部分组织中的 B 细胞。当药物代谢完毕后,骨髓中新生的、健康的 B 细胞重新占据生态位,从而消除了产生自身抗体的源头。
3. 近期核心 BD 授权与并购交易 (2024 - 2026)
TCE 的高技术壁垒使得大药企(MNC)高度依赖外部“技术购买”来补充管线。2025-2026年的交易热点明显向“自免跨界”和“掩蔽降毒技术”倾斜:
| 交易时间 | 收购方 / 授权方 | 被收购方 / 标的 | 核心靶点与技术 | 交易金额 (首付 + 里程碑) | 战略意义 |
| 2026年3月 | UCB (优时比) | Antengene (德琪医药) | ATG-201 (CD19 x CD3)搭载掩蔽降毒技术 | 8000万美元首付总计约 11.8亿美元 | UCB 借此重磅切入自身免疫疾病的 TCE 赛道。 |
| 2026年2月 | Astellas (安斯泰来) | Vir Biotechnology | VIR-5500 (PSMA x CD3)PRO-XTEN® 双重掩蔽技术 | 3.35亿美元首付总计约 17亿美元 | 押注下一代前列腺癌的低毒性肿瘤微环境激活技术。 |
| 2024-2025年 | Merck (默沙东) | Harpoon Therapeutics | HPN328 (DLL3 x CD3)TriTAC 三特异性技术 | 全现金收购,总价 6.8亿美元 | 巩固默沙东在小细胞肺癌和神经内分泌肿瘤领域的管线深度。 |
| 2024-2025年 | Context Therapeutics | BioAtla | BA3362 (Nectin-4 x CD3) | 1500万美元首付总计 1.33亿美元 | 应对 Nectin-4 ADC(如 Padcev)耐药后的实体瘤患者群体。 |
二、拆解“掩蔽降毒技术 (Masking Technology)”的分子设计原理
实体瘤 TCE 研发面临的最大死局是 On-target Off-tumor(靶向正确但脱离肿瘤区域)的毒性。许多实体瘤抗原(如 EGFR、HER2、PSMA)在正常组织中也有少量表达。第一代 TCE 在外周血中一旦遇到正常细胞上的抗原,就会拉拽 T 细胞进行“误杀”,引发致命的全身性免疫风暴 (CRS)。
掩蔽技术(又称前体药物Prodrug 技术)应运而生。其核心设计理念是:让武器在平民区处于“锁定”状态,只有进入敌占区(肿瘤微环境,TME)才拔下保险销。
1.掩蔽分子的“三位一体”核心构造
一个典型的掩蔽型 TCE 分子通常由以下三个精密模块构成:
模块 A:掩蔽肽 (The Masking Peptide)
原理:这通常是一段空间构象或氨基酸序列经过特殊设计的短肽。它被放置在抗 CD3 结合域(有时也放在抗肿瘤抗原结合域)的外部。
作用:通过空间位阻(物理遮挡)或弱亲和力结合(化学遮挡),占据抗体的抗原结合位点 (CDR 区)。这样,在血液循环中,TCE 无法结合外周血中的 T 细胞,从而实现“休眠”。
模块 B:肿瘤微环境特异性可底物裂解连接子(Cleavable Linker)
原理:这是连接“掩蔽肽”和“核心双抗体”的铰链。它是一段特异性的氨基酸序列,专门作为某些特定蛋白酶的“底物”。
作用:肿瘤组织在快速生长和侵袭时,会大量分泌特定的蛋白酶(如基质金属蛋白酶 MMP2/9、尿激酶 uPA、成纤维细胞活化蛋白 FAP 等)。这些蛋白酶在正常组织和血液中含量极低。当掩蔽 TCE 流经肿瘤时,这些特异性蛋白酶会精准剪断这个 Linker。
模块 C:半衰期延长结构域 (Half-life Extension Domain)
原理:由于加上了掩蔽肽,分子往往面临不稳定或易被肾脏快速清除的问题。
作用:通常通过融合 XTEN 聚合物(如前文提到的 Vir Biotechnology的 PRO-XTEN 技术)、白蛋白结合域或 Fc 区域,增大分子量,确保其在血液中存留足够长的时间,以便巡航并积聚到肿瘤部位。
2.掩蔽技术的“拔栓”全过程 (Action Mechanism)
静默巡航(Systemic Circulation):药物注射入血。由于“掩蔽肽”的遮挡,TCE 无法结合循环系统中的正常 T 细胞或表达微量抗原的正常组织。全身毒性(CRS、神经毒性)被降至极低。
富集与切割(Accumulation & Cleavage):大分子药物通过高通透性和滞留效应 (EPR) 渗入肿瘤微环境。此时,TME 中高浓度的肿瘤特异性蛋白酶(如 MMPs 或 uPA)识别出“可裂解连接子”并将其切断。
脱面具激活(Unmasking & Activation):连接子断裂后,“掩蔽肽”脱落并随血流代谢掉。原本被遮挡的 CD3 结合域暴露出来,恢复 100% 的亲和力。
精准定点爆破(Targeted Killing):激活后的 TCE 迅速在肿瘤局部将 T 细胞与肿瘤细胞拉近,形成免疫突触,释放颗粒酶和穿孔素,完成肿瘤的定点清除。
3.掩蔽技术的代表性平台
CytomX的 Probody 技术:该领域的先驱,采用肽段掩蔽,广泛应用于 ADC 和双抗。
Amunix的 XTEN 掩蔽(现属赛诺菲):利用高度亲水、非免疫原性的长链氨基酸聚合物 (XTEN)形成巨大的空间位阻来进行掩蔽,半衰期极长。
BioAtla的 CAB (条件活性生物制剂) 技术:这是另一种思路的“掩蔽”。它不依赖蛋白酶切割,而是依赖pH值响应。正常组织 pH 值为中性(药物不结合),而肿瘤微环境因乳酸堆积呈微酸性(pH 6.0-6.5),抗体在酸性环境下构象改变,恢复结合力。
三、TCE与 CAR-T 在自免领域的全方位对比
| 评估维度 | TCE (T 细胞衔接器) | CAR-T (嵌合抗原受体 T 细胞疗法) | 自免领域的优劣势定论 |
| 药物属性 | 现货型 (Off-the-shelf) 标准化抗体蛋白。 | 自体活细胞药物 (Autologous living drug),需定制化生产。 | TCE 完胜。自免患者基数庞大,TCE 能够随取随用,满足大规模临床需求。 |
| 生产周期与成本 | 生产周期极短(传统抗体工艺),单疗程成本预期在数万人民币/几千美元量级。 | 需采血、基因改造、扩增,周期通常需 2-4 周,单次成本高达数十万甚至上百万人民币。 | TCE 完胜。自免疾病并非绝症,医保和患者极难承受 CAR-T 的天价。 |
| 安全性与毒性可控性 | 半衰期相对较短。若发生严重不良反应(如 CRS),可通过停药迅速控制。 | 活细胞在体内扩增,一旦输入难以“撤回”。部分患者可能出现较长时间的血细胞减少或中枢神经毒性 (ICANS)。 | TCE 更具优势。自免患者对安全性的容忍度远低于晚期癌症患者,TCE 的“可逆性”是巨大加分项。 |
| 组织穿透与清除深度 | 依赖大分子抗体的物理弥散,对淋巴结深处或组织驻留 B 细胞的清除可能不如活细胞彻底。 | 活细胞具有“主动趋化和归巢”能力,且能在体内扩增,组织穿透力极强。 | CAR-T 占优。对于某些深部组织纤维化的自免疾病,CAR-T 能够实现更深度的 B 细胞耗竭。 |
| 长期持久性 | 药物代谢后,杀伤作用停止。若自免复发,可能需要重复给药。 | CAR-T 细胞可能在体内形成记忆细胞,存活数月乃至数年,提供长效监视。 | 各有千秋。TCE 易于重复给药;CAR-T 追求“一劳永逸”,但长效 B 细胞缺失也会增加重度感染风险。 |
自免 TCE 总结:TCE 牺牲了 CAR-T 极致的“深度与长效”,换取了压倒性的“安全性、低成本和普适性”。目前,包括罗氏的 Glofitamab (CD20xCD3)、安进的Blinatumomab (CD19xCD3) 等均已开启自免适应症的临床探索,这也是近期大型药企疯狂扫货此类管线的原因。
四、总结
TCE技术正在经历一场深刻的蜕变:
适应症维度的降维打击:从血液瘤的最后一道防线,向前线治疗推移;从攻克冷实体瘤,到跨界进入百亿美元级别的自身免疫性疾病市场。
分子设计的底层逻辑重构:早期的 TCE 追求“极致杀伤(高亲和力)”,而如今的研发重点已全面转向“可控与降毒(掩蔽技术、低亲和力、共刺激)”,以扩大治疗窗口。如果说 TCE 进军自免疾病是“降维打击”,那么掩蔽技术就是实体瘤 TCE 突围的“防弹衣”。这两种趋势正在重塑 2026 年以来的创新药投融资格局。