来源:抗体圈
摘要:抗体药物偶联物(ADCs)为妇科恶性肿瘤的治疗带来了新的希望。本文详细介绍了 ADCs 的作用机制、在多种妇科癌症中的临床应用,包括已获 FDA 批准的药物(如 Mirvetuximab soravtansine、Tisotumab vedotin、Trastuzumab deruxtecan)以及正在研究的 Trop-2 ADCs 等其他 ADCs。同时,探讨了 ADCs 的毒性特点、耐药问题、成本效益,并指出通过生物标志物选择患者和合理安排治疗顺序,对优化 ADCs 治疗效果至关重要 。
一、ADCs:妇科癌症治疗的新希望
在妇科癌症治疗领域,传统的化疗和免疫治疗虽然取得了一定进展,但仍面临肿瘤异质性、耐药和不良反应等挑战。抗体药物偶联物(ADCs)作为一种新型药物,由单克隆抗体、细胞毒性有效载荷和连接子组成,能够精准地将细胞毒性药物输送到肿瘤细胞,提高治疗效果,同时减少对正常组织的损伤,为患者带来了新的希望 。然而,ADCs 在应用中也存在一些问题,比如肿瘤异质性导致疗效差异、耐药性的产生、独特的毒性反应以及高昂的生产成本等。因此,了解 ADCs 的作用机制、临床应用效果、毒性特点以及如何克服这些问题,对提高妇科癌症的治疗水平至关重要 。
二、ADCs 的作用机制与特点
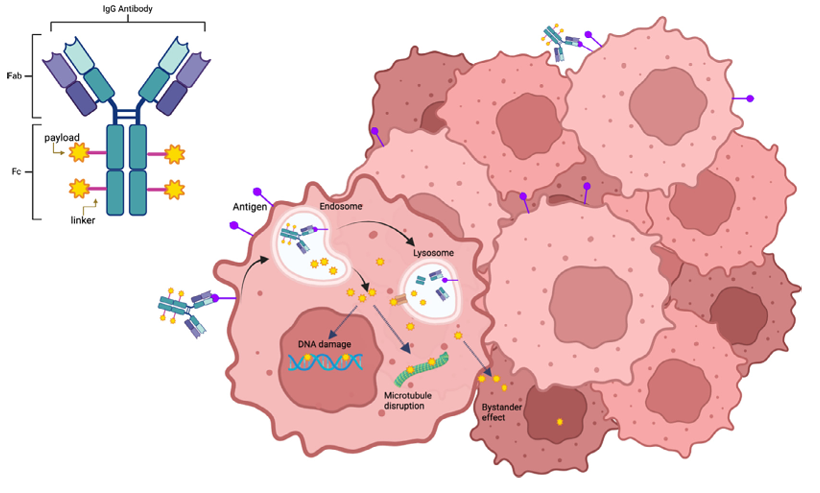
- 作用机制:ADCs 的单克隆抗体部分能够特异性地识别肿瘤细胞表面的抗原,然后通过内吞作用进入细胞。在细胞内,连接子会在特定条件下断裂,释放出细胞毒性有效载荷,这些有效载荷能够干扰肿瘤细胞的 DNA 复制、微管形成等关键过程,从而杀死肿瘤细胞(展示 ADCs 作用机制的图 1,更直观地呈现这一过程 )。此外,一些有效载荷还能产生旁观者效应,杀死周围未表达靶抗原的肿瘤细胞。
- 毒性机制与耐药性:尽管 ADCs 能减少对健康细胞的药物暴露,但仍会产生一些毒性反应。一方面,它可能导致与传统化疗相似的毒性,如神经病变;另一方面,还会出现一些独特的副作用,像出血、口腔炎、眼部毒性和间质性肺病等 。ADCs 的耐药机制较为复杂,肿瘤细胞可能对其各个组成部分产生耐药,包括抗原表达缺失、药物运输障碍、溶酶体功能异常以及对有效载荷的耐药等 。
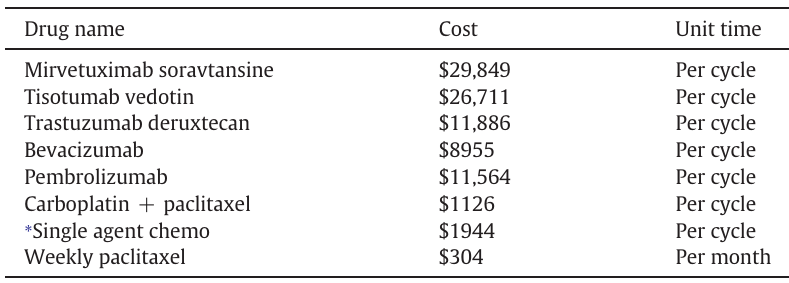
- 成本效益:ADCs 的研发和生产过程复杂,导致其成本较高。与传统治疗方法相比,ADCs 的治疗费用昂贵,这限制了其在一些资源有限地区的可及性。例如,使用 Mirvetuximab soravtansine 治疗铂耐药卵巢癌的每月费用远高于传统的紫杉醇和贝伐单抗联合治疗(关于 ADCs 与常用系统性治疗费用比较的表格 1,让读者更清晰地了解成本差异 )。
三、FDA 批准的 ADCs 在妇科癌症中的应用
1.铂耐药卵巢癌的新选择 ——Mirvetuximab soravtansine:Mirvetuximab soravtansine(MIRV)主要针对叶酸受体 α(FRα)阳性的肿瘤细胞。在铂耐药的卵巢癌治疗中,多项临床试验显示出其良好的疗效。例如,在 FORWARD-1 试验中,虽然整体无进展生存期(PFS)未显著改善,但客观缓解率(ORR)有所提高,且在高 FOLR1 表达的亚组中总生存期(OS)有优势 。在 SORAYA 试验和 MIRASOL 试验中,MIRV 也表现出了一定的疗效,基于这些结果,MIRV 获得了 FDA 的加速批准和完全批准。MIRV 的常见副作用包括胃肠道反应、周围神经病变和眼部毒性等,不过通过一些缓解策略,如眼部检查和使用眼药水等,可以减轻这些不良反应(关于 MIRV 眼部缓解策略的表格 2,展示具体的应对措施 )。
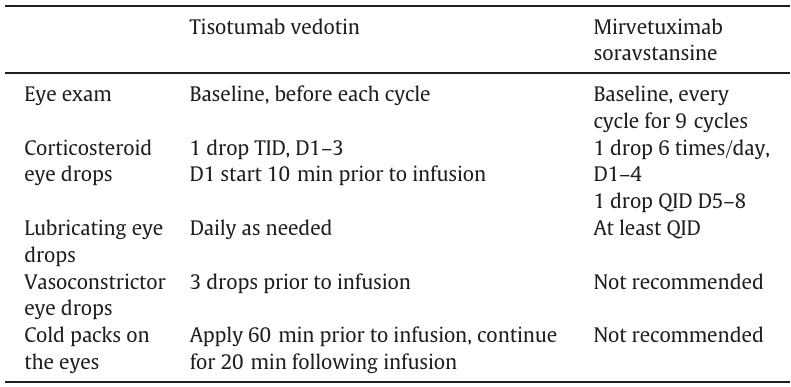
2.宫颈癌治疗的新突破 ——Tisotumab vedotin:Tisotumab vedotin(TV)以组织因子(TF)为靶点,在宫颈癌治疗中展现出了潜力。innovaTV-204 试验表明,TV 作为二线或三线单药治疗,能为复发 / 转移性宫颈癌患者带来一定的缓解率 。后续的 InnovaTV-205 试验和 InnovaTV-301 试验进一步证实了其联合治疗的有效性,TV 联合其他药物(如卡铂、帕博利珠单抗、贝伐单抗)可提高缓解率,延长患者生存期。TV 的毒性反应包括眼部毒性、出血事件和周围神经病变等。眼部毒性较为常见,通过类似 MIRV 的眼部护理方案可进行缓解(文中关于 TV 和 MIRV 眼部缓解策略的表格 2 );出血事件与 TF 干扰凝血级联有关,严重出血时需停药;周围神经病变则与药物有效载荷抑制微管的特性有关。基于这些试验结果,TV 获得了 FDA 的完全批准,成为宫颈癌二线治疗的重要选择 。
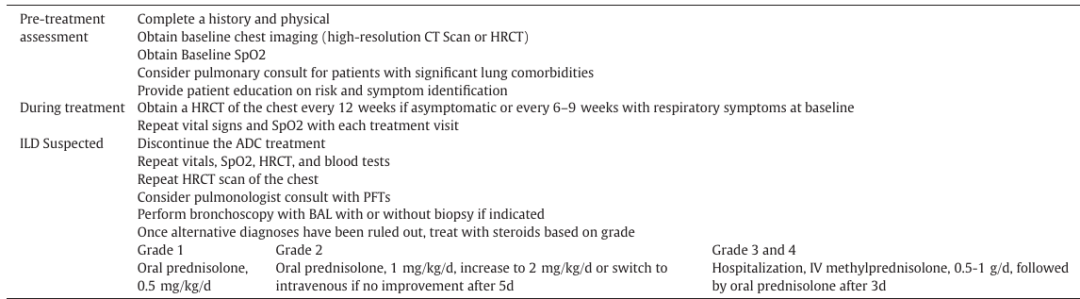
3.HER2 阳性恶性肿瘤的有效药物 ——Trastuzumab deruxtecan:Trastuzumab deruxtecan(T-Dxd)靶向人表皮生长因子 2(HER2),HER2 在多种妇科癌症(如子宫内膜癌、卵巢癌、宫颈癌等)中存在不同程度的表达 。DESTINY-PanTumor02 试验显示,T-Dxd 对 HER2 阳性的晚期转移性实体瘤患者有较好的疗效,在不同妇科癌症亚组中也有显著的缓解率。不过,T-Dxd 也有一些副作用,最值得关注的是间质性肺病(ILD)和肺炎,此外还包括贫血、疲劳、恶心呕吐等。治疗前需要进行胸部影像学检查、肺功能测试等筛查,治疗过程中若出现 ILD,需根据严重程度调整剂量或停药(关于 T-Dxd 的 ILD 评估 / 管理的表格 3,详细展示应对流程 )。基于试验结果,FDA 加速批准 T-Dxd 用于治疗无法切除或转移性 HER2 阳性实体瘤患者,但目前标签限制为 IHC3 + 患者 。
四、新兴的 Trop-2 ADCs 在妇科癌症中的研究
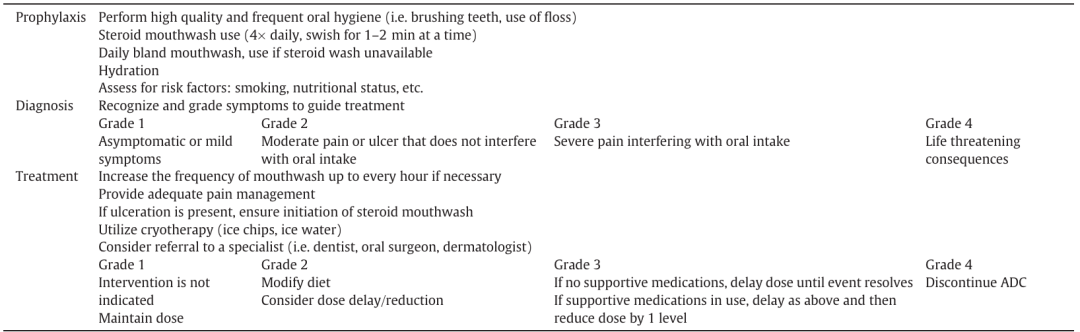
- Trop-2 ADCs 概述:Trophoblast cell surface antigen - 2(Trop-2)是一种在多种妇科恶性肿瘤中高表达的跨膜糖蛋白,成为了 ADC 治疗的一个重要靶点。目前针对 Trop-2 的 ADCs 在多种妇科癌症的治疗研究中展现出了一定的前景,但由于 Trop-2 在正常上皮组织也有表达,使用这类 ADCs 可能会导致粘膜炎和口腔炎等副作用(关于 Trop-2 ADCs 导致粘膜炎和口腔炎的处理建议表格 4,展示应对策略 )。
- 在不同妇科癌症中的应用及进展
- 子宫内膜癌:Trop-2 在子宫内膜癌中高表达。Sacituzumab govitecan(SG)、Sacituzumab tirumotecan(sac-TMT)和 Datopotamab deruxtecan(Dato-DXd)等针对 Trop-2 的 ADCs 在子宫内膜癌的治疗研究中均有开展。例如,SG 在相关试验中显示出一定的缓解率,目前还有多项针对复发子宫内膜癌的临床试验正在进行,旨在比较这些 ADCs 与传统治疗方案的疗效 。
- 宫颈癌:Trop-2 在宫颈癌中也有较高表达。在相关临床试验中,Sac-TMT 联合帕博利珠单抗治疗复发宫颈癌展现出了较好的临床活性,目前也有随机 3 期试验正在开展,对比 Sac-TMT 与医生选择的治疗方案(如培美曲塞、Tisotumab vedotin 等)的疗效 。
- 卵巢癌:Trop-2 在卵巢癌中同样广泛表达。Dato-DXd 在卵巢癌的 2 期临床试验中显示出对铂敏感和铂耐药卵巢癌患者的缓解率,为卵巢癌的治疗提供了新的选择方向 。
五、其他 ADCs 的研究现状
除了上述药物,还有一些 ADCs 也在妇科癌症治疗领域进行研究。比如,IBI354 针对 HER2 受体,在局部晚期 / 不可切除或转移性妇科实体瘤的 1 期研究中显示出一定的疗效和可接受的安全性 ;Rinatabart sesutecan(Rina-S)靶向 FRα,在卵巢癌和子宫内膜癌的 1/2 期研究中也取得了不错的结果;Raludotatug deruxtecan(R-DXd)以 Cadherin 6(CDH6)为靶点,在卵巢癌的 1 期研究中展现出了较好的缓解率,目前还有全球 2/3 期试验正在进行,进一步评估其疗效和安全性 。
六、总结与展望
ADCs 为妇科癌症治疗带来了新的方向和希望,已获批的药物在临床实践中取得了一定的成效,新兴的 ADCs 也展现出了潜在的治疗价值。然而,ADCs 在临床应用中仍面临一些挑战,如独特的毒性反应、高昂的成本以及耐药性等问题。未来,需要进一步探索有效的生物标志物,以更精准地筛选适合接受 ADCs 治疗的患者,提高治疗效果并减少不良反应 。同时,合理安排 ADCs 与其他治疗方法的顺序,以及优化 ADCs 的设计和生产工艺,降低成本,将有助于推动 ADCs 在妇科癌症治疗领域的广泛应用,为更多患者带来生存获益 。