随着生物医药技术的迅猛进步,哺乳动物细胞系因其连续传代的特性,在疫苗和治疗性生物制品的生产中发挥着日益重要的作用。然而,这种生产过程中不可避免地会涉及宿主细胞和病毒残余DNA的传递问题,进而可能给受种者带来癌基因激活和病毒感染的风险。因此,核酸残留问题成为了药品监管部门关注的焦点,特别是关于其安全性评价。
残留DNA(rDNA)的潜在危害不容忽视。其中,感染性rDNA指的是那些能够整合到染色体外或存在于其中的DNA病毒,以及反转录病毒中的潜在前病毒基因组。这些感染性成分可能直接对受种者的健康构成威胁。此外,rDNA还可能具有致瘤性,这主要是通过两种机制实现的:一是引入显性致癌基因,如myc和ras等,导致正常细胞分化异常,进而可能产生致瘤性;二是rDNA的插入可能引起正常细胞的基因突变。尽管由于DNA整合频率相对较低,这种致癌现象并不常见,但一旦发生,后果可能是严重的。
除了感染性和致瘤性,rDNA还可能引发免疫原性反应。这种免疫原性往往来自于细菌DNA中富含的CpG序列。当这些序列进入人体后,可能触发免疫系统的反应,导致不必要的健康风险。
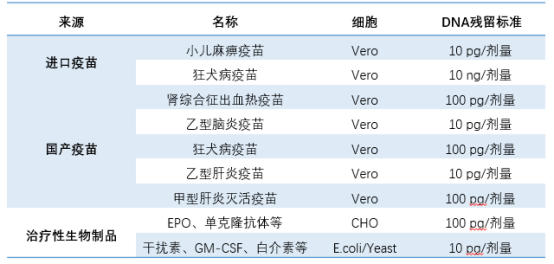
鉴于rDNA的这些潜在危害,生物制品生产过程中对残留核酸的检测和去除显得尤为重要。世界卫生组织(WHO)及各国药物监管机构均对此有明确规定,要求用于治疗用途的重组生物制品中的核酸污染应严格控制在一定范围内。一般来说,每剂最终产品中的核酸污染应限制在100 pg以下,特殊情况下也不得超过10 ng。
为了实现这一目标,生物制品生产企业需要采取一系列措施,包括优化生产工艺、加强原材料的质量控制、采用高效的核酸去除技术等。同时,监管部门也应加强监管力度,确保企业严格按照规定进行生产,以保障公众用药安全。
综上所述,生物医药技术的发展为疫苗和治疗性生物制品的生产提供了更多可能性,但同时也带来了新的挑战。对于rDNA等核酸残留问题,我们需要从多个方面入手,加强研究和监管,确保生物制品的安全性和有效性。
表1:我国部分疫苗及治疗用生物制品残余DNA标准
鉴于rDNA去除过程中遇到的聚集、包裹以及沉淀等挑战,传统的去除方法效率确实不尽如人意,而酶解法尽管有效,但操作复杂且条件难以稳定。因此,寻找一种高效且易于操作的核酸去除方法显得尤为重要。
逐典Pannarase全能核酸酶作为一种非特异性核酸内切酶,展现出了独特的优势。其来源于Serratia marcescens,能够在多种条件下高效降解各种形式的DNA和RNA,生成特定大小的寡核苷酸残基片段。这种酶对核酸碱基序列没有特异性要求,意味着它可以在核酸链内的任意位置进行切割,从而大大提高了去除残留核酸的效率。
逐典Pannarase全能核酸酶优势:
1.无动物源性、无氨苄青霉素
2.杰出单位比酶活、更高效的核酸降解能力
3.先进的生产工艺,非传统His标签纯化、排除引入金属离子风险
4.严格的质控标准,内毒水平低,确保单位酶活的准确性以及批次间稳定性
全能核酸酶应用条件:
全能核酸酶的酶活会受到多种因素的影响(例如温度、pH、离子强度等),故用量范围也会从0.1 U/mL-250 U/mL不等。因此,不同的操作环境下酶的最佳浓度不同,需要通过实验设置梯度进行最佳条件的摸索。
应用实例:
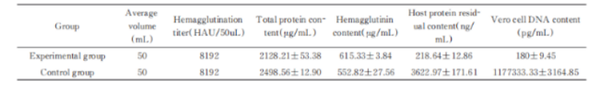
1.样品:狂犬病毒浓缩液
处理条件:核酸酶浓度50~90U/ml ,
37 ℃处理 2 h,转入18 ~ 26 ℃处理 6h
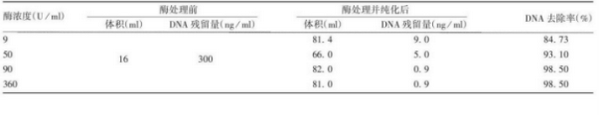

2.样品:狂犬病病毒浓缩液
处理条件:25、50和100 U/ml,37℃
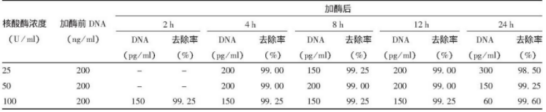

3.样品:流感病毒浓缩液
处理条件:10 U/mL,37℃